Efecto antimicrobiano de tres aceites esenciales de la familia Lamiaceae para el control Ralstonia solanacearum
Antimicrobial effect of three essential oils from the Lamiaceae family for control Ralstonia solanacearum
Jovanna Acero-Godoy1, Tomás de Jesús Guzmán-Hernández2, Wilman Antonio Delgado-Ávila3, Johan Steven Alcántara-Cortés4, Mauricio Soto-Suárez5, Elizabeth Gil-Archila6
Fecha de recepción: 19 de setiembre, 2024
Fecha de aprobación: 20 de enero, 2025
Acero-Godoy, J; Guzmán-Hernández, T.J; Delgado-Ávila, W.A; Alcántara-Cortés, J.S; Soto-Suárez, M; Gil-Archila, E. Efecto antimicrobiano de tres aceites esenciales de la familia Lamiaceae para el control Ralstonia solanacearum. Tecnología en Marcha. Vol. 38, No 3. Julio-Setiembre, 2025. Pág. 54-68. https://doi.org/10.18845/tm.v38i3.7511
https://doi.org/10.18845/tm.v38i3.7511
Palabras clave
Bioplaguicidas; concentración mínima bactericida (CMB); concentración mínima inhibitoria (CMI); Ralstonia solanacearum; Origanum majorana; Rosmarinus officinalis; Thymus vulgaris.
Resumen
Rosmarinus officinalis L., Origanum majorana L. y Thymus vulgaris L., son plantas aromáticas que pertenecen a la familia Lamiaceae, sus aceites esenciales han sido ampliamente estudiados como sustancias antimicrobianas de bacterias fitopatógenas entre las que se encuentra Ralstonia solanacearum. El objetivo de la presente investigación fue determinar la composición química de los aceites esenciales y la actividad antimicrobiana contra R. solanacearum. Los aceites esenciales (AE) fueron obtenidos de hojas y tallos por el método de arrastre con vapor y la composición química por medio de CG-MS. Se determinó la concentración mínima inhibitoria (CMI) y concentración mínima bactericida (CMB) para cada uno de los aceites esenciales. El compuesto mayoritario para O. majorana y T. vulgaris fue g-terpineno (17,32 %, 33,47 % respectivamente) y para R. officinalis a-pineno (22,47%). La densidad promedio de los tres aceites esenciales fue 0,85 mg/mL y el mayor rendimiento de los aceites esenciales se obtuvo para R. officinalis 0,86 % (% p/p). Los tres aceites esenciales generaron efecto tanto inhibitorio como bactericida contra R. solanacearum; para O. majorana, T. vulgaris y R. officinalis con CMI de 0,545 mg/mL, 0,625 mg/mL y 1,09 mg/mL respectivamente y el valor de las CMB 1,09 mg/mL, 1,25 mg/mL y 2,18 mg/mL, respectivamente. Los resultados obtenidos permiten proponer el uso de los aceites esenciales como posibles bioplaguicidas como una alternativa para disminuir el uso de químicos sintéticos convencionales, mitigando el impacto que estos producen en aguas, suelos y en el consumidor final; el ser humano.
Keywords
Biopesticides; minimum bacterial concentration (MBC); minimum inhibitory concentration; Ralstonia solanacearum; Origanum majorana; Rosmarinus officinalis; Thymus vulgaris.
Abstract
Rosmarinus officinalis L., Origanum majorana L., and Thymus vulgaris L. are aromatic plants that belong to the Lamiaceae family. Their essential oils have been widely studied as antimicrobials against phytopathogenic bacteria, including R. solanacearum. The objective of the present investigation was to determine the chemical composition of essential oils and the antimicrobial activity against R. solanacearum. The essential oils were obtained from leaves and stems by Steam distillation method, and chemical composition was determined using CG-MS; Minimum inhibitory concentration (MIC) and minimum bactericidal concentration tests were developed for each essential oil. Most found compounds for O. majorana and T. vulgaris were g-terpinene 17,32 %, and 33,47 % respectively for R. officinalis a-pinene 22,47 %. The average density of three essential oils was 0,85 mg/mL, and the highest essential oil (EO) yield was obtained for R. officinalis 0,86 % (% w/w). All essential oils generated both inhibitory and bactericidal effects against R. solanacearum: for O. majorana, T. vulgaris, and R. officinalis the MIC were 0,545 mg/mL, 0,625 mg/mL, and 1,09 mg/mL respectively and the MBC value was 1,09 mg/mL, 1,25 mg/mL and 2,18 mg/mL respectively. These results allow us to propose using essential oils as biopesticides as an alternative to reduce the application of conventional synthetic chemicals, mitigating the impact that these produce on water, soil, and the final consumer, humans.
Introducción
Ralstonia solanacearum antes conocida como Pseudomona solanacearum es considerada como un complejo de especies (RSSC) filogenéticamente relacionadas, fitopatógenas y cosmopolita con un alto impacto en la agricultura en cultivos de importancia económica como tomate, papa y banano, produciendo marchitamiento bacteriano en plantas solanáceas, podredumbre negra en papa y enfermedad de moko en plátano. Su difícil erradicación ha dificultado el desarrollo de estrategias de control efectivas entre las que se han implementado el uso de métodos químicos tipo plaguicidas, tratamientos físicos como solarización, prácticas culturales como rotación de cultivos y el control biológico tanto con microorganismos o con derivados de plantas como los aceites esenciales [1], [2].
La familia Lamiácea antiguamente llamada Labiatae es una de las familias botánicas más numerosas representada por hierbas, plantas herbáceas, arbustos o especies de árboles distribuidos en 240 géneros y casi 7000 especies, ampliamente distribuidas en el mundo a diferentes alturas entre las cuales sobresalen el tomillo, orégano y romero. Al igual que otras plantas aromáticas posee compuestos bioactivos como terpenoides, alcaloides, fenilpropanoides, fenoles, ésteres, cetonas, ácidos orgánicos encontrados en los aceites esenciales de las mismas que son sustancias aromáticas y volátiles ubicadas en diferentes partes de la planta como hojas, flores raíces, semillas frutos y cuya concentración de compuestos puede variar dentro de la misma especie dependiendo de factores ambientales, edad del cultivo, condiciones edafoclimáticas, método de recolección y extracción, que se han convertido en una alternativa viable para el desarrollo de nuevas sustancias que pueden ser utilizadas como antioxidantes, antiinflamatorios, antivirales, antifúngicos, antibacteriales entre muchas otras propiedades que poseen. La capacidad antibacterial de los aceites esenciales de plantas como Origanum majorana L., Rosmarinus officinalis L. y Thymus vulgaris L., ha sido demostrada contra microorganismos de interés clínico como Escherichia coli, Staphylococcus epidermidis, Salmonella enteritidis, Klebsiella pneumoniae, Saprolegnia parasitica y fitopatógenos como Pseudomonas syringae pv. phaseolicola. Por las anteriores razones el objetivo del presente trabajo es determinar el potencial antimicrobiano de los aceites esenciales de Origanum majorana L., Rosmarinus officinalis L. y Thymus vulgaris L. extraídos por el método de arrastre con vapor, su caracterización química, rendimientos y la concentración mínima inhibitoria (CMI) y concentración mínima bactericida (CMB) para establecer si presentan actividad antimicrobiana contra el fitopatógeno Ralstonia solanacearum, como posible alternativa a los métodos de control alternativos a los plaguicidas convencionales que generan una alta contaminación en el medio ambiente [3], [4], [5], [6], [7], [8].
Materiales y métodos
Material vegetal e identificación taxonómica
Las hojas de cada especie se adquirieron en el centro de acopio “la plaza de mercado Samper Mendoza”, (Bogotá, Colombia), el material provino en su totalidad de la sabana de Bogotá y siempre fue adquirido con el mismo proveedor. Un ejemplar de cada especie se depositó en el Herbario Nacional Colombiano para su determinación, bajo los códigos: COL 616745 para Origanum majorana, COL 612138 para Rosmarinus officinalis L. y COL 612139 para Thymus vulgaris L
Extracción y rendimiento de los aceites esenciales
Para la obtención de los aceites esenciales, las hojas del material vegetal fresco de cada planta fueron sometidas a destilación por arrastre con vapor en un equipo de destilación que comprendía un vaso de extracción de 12 litros, una caldera o alambique y una trampa tipo Clevenger para la recolección y separación de los aceites esenciales para luego ser conservados con sulfato de sodio (Na2SO4) y mantenidos a -10º C.
El rendimiento de los aceites esenciales con respecto a su biomasa vegetal se calculó por medio de la ecuación:
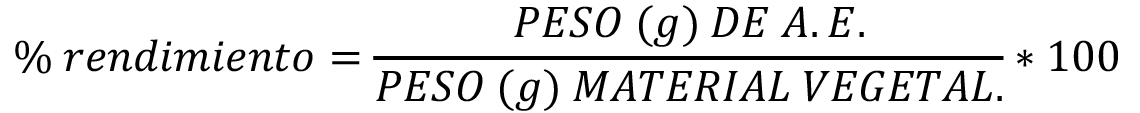 (Ecuación 1)
(Ecuación 1)
Donde, peso (g) de A.E. son los gramos del aceite esencial obtenido y peso (g) del material vegetal corresponde al peso en gramos del material vegetal fresco [9].
Densidad relativa del aceite esencial 20º C e índice de refracción:
La densidad se determinó mediante el método oficial AOAC 940.28 de 1990; se utilizó un picnómetro de 1,0 ml de capacidad, el cual fue pesado vacío después, se llenó con 1,0 ml del aceite esencial, se pesó el conjunto y por diferencia de pesos se determinó la densidad relativa del aceite esencial empleando la ecuación 2 [10].
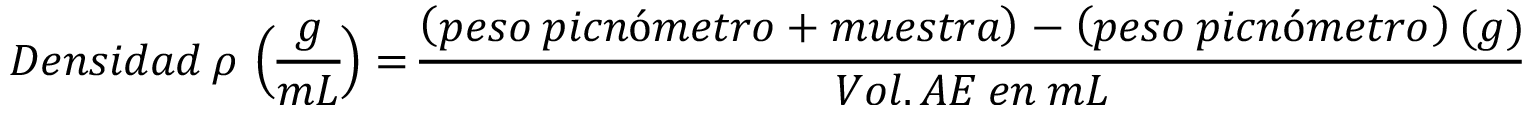 (Ecuación 2)
(Ecuación 2)
Para el índice de refracción se utilizó el método oficial AOAC 919.28:1990. La prueba fue realizada utilizando un refractómetro (Sper Scientific), se adicionaron 50 mL del aceite esencial en el prisma a 20 °C y se realizó la lectura [10].
Cromatografía Gases acoplada a Espectrometría de Masas (GC-MS)
Los aceites esenciales obtenidos se analizaron en un cromatógrafo de gases Shimadzu GC 2010, con inyector split/splitless acoplado a un detector selectivo de masas MS/GCT 8040, modo de ionización EI, analizador de masas triple cuadrupolo y dos sistemas de separación. El primero empleó una columna apolar RTX-5MS (60 m x 0,25 mm x 0,25 μm) bajo las siguientes condiciones de operación: el gas de arrastre fue helio a un flujo de 1,5 ml/min. La temperatura del horno se programó desde 40 °C (2 min) hasta 125 °C (2 min) a 4 °C/min, luego se incrementó hasta 160 °C (5 min) a 4 °C/min, posteriormente se aumentó hasta 220 °C (8 min) a 5 °C/min y, finalmente, la temperatura aumentó a 280 °C (4 min) a 5 °C/min. La temperatura en el puerto de inyección fue de 250 °C y la de la línea de transferencia de 290 °C, la relación de split 1:20 y el voltaje de ionización fue de 70 eV a una corriente de 60 μA. La adquisición de los espectros de masas se realizó en un rango de masas entre 30-600 m/z. El segundo sistema de separación fue una columna polar DB-WAX (60 m×0,25 mm×0,25 μm) operado bajo las mismas condiciones excepto por la programación de la temperatura del horno que fue de la siguiente forma: 45 °C (4 min) hasta 250 °C (8 min) a 4 °C/min. Se inyectó 1,0 μl de cada solución analizada. Dilución 1/40 (25 μl aceite a 1.0 ml utilizando hexano como diluyente).
La identificación de los compuestos se basó en la comparación de los índices de retención (IR) y sus espectros de masas con los reportados en las librerías NIST08, Wiley 9L, Pherobase y en Adams [11]. Los IR se calcularon teniendo en cuenta los tiempos de retención de una serie homóloga de n-alcanos (C8 – C 28) corridos bajo las mismas condiciones de análisis cromatográficas que el aceite esencial. La integración de la corriente iónica total, expresada en porcentaje de abundancia, se utilizó como un parámetro aproximado para determinar la composición relativa del aceite.
Cepa de Ralstonia solanacearum
La bacteria Ralstonia solanacearum fue registrada en el Registro Nacional de Colecciones (RNC129) y colectada bajo el permiso marco número 1466 de Agrosavia de 2014, actualizado por la resolución 04039 del 19 de julio de 2018. pertenece a un aislamiento obtenido de tomate que estaba conservada a -80º C en glicerol, y según la caracterización molecular pertenece al filotipo americano II. La bacteria fue activada en medio TZC durante 48 a 72 horas a 28º C [12].
Método de difusión en agar
La actividad antimicrobiana de cada aceite esencial se evaluó por medio del método de difusión en pozo (perforación en gel de agar), en el cual se realizaron 6 perforaciones con un diámetro de 5,0 mm; la cepa de R. solanacearum se homogenizó en caldo nutritivo hasta alcanzar una concentración de 1*108 UFC/ml y se inoculó en la superficie de todo el medio; en cada uno de los pozos se colocaron 20 μl de los diferentes aceites esenciales a 24 concentraciones diferentes (500, 280, 240, 200, 180, 160, 140, 120, 100, 80, 60, 50, 40, 20, 10, 5.0, 2.0, 1.0, 0.5, 0.25, 0,10, 0,05, 0,025, 0,01 mg/mL), los aceites esenciales se diluyeron con acetona al 99%, como controles negativos se utilizó acetona y agua destilada, y como control positivo rifampicina; una vez inoculadas las cajas, se incubaron a 28º C durante 24 a 48 horas, posterior a la incubación se midió el halo de inhibición del crecimiento (mm) y se calculó para cada aceite esencial el porcentaje de efecto inhibitorio relativo, con respecto al control positivo con la siguiente ecuación [13], [14].
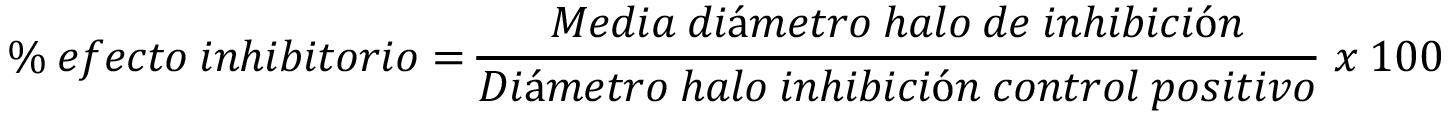 (Ecuación 3)
(Ecuación 3)
Determinación de Concentración mínima inhibitoria (CMI) y concentración mínima bactericida (CMB), método micro dilución
La CMI es la concentración más baja de la sustancia que puede inhibir el crecimiento visible de un microorganismo después de incubar durante 24 horas y la CMB es la concentración más baja que puede inhibir el crecimiento de un microorganismo después de ser subcultivado en un medio libre del compuesto evaluado. Para realizarlo se utilizó el método de microdilución (ISO 10932, IDF 223:2010) se suspendió una colonia de bacterias en 5,0 ml de caldo nutritivo y se incubó a 28º C durante 24 horas en agitación, después se realizó una dilución para obtener un valor de absorbancia en el espectrofotómetro que correspondía a una concentración de 1,5*108 UFC/ml (0,1 D.O a 600 nm). Se prepararon una serie de diluciones de los aceites esenciales con acetona, y en una caja de Elisa de 96 pozos con un volumen final de trabajo de 200 μl, se colocaron 2,0 μl del microorganismo para obtener una concentración final de 1,0*106 ufc/ml y 10 μl del aceite esencial diluido, además de caldo nutritivo como medio de crecimiento; como control positivo se utilizó R. solanacearum con el medio de cultivo únicamente, como control negativo se utilizó el microorganismo con el medio de cultivo (caldo nutritivo) y rifampicina 5,0 μg/ml; se evaluó además la acetona para determinar que no generará inhibición en el crecimiento de la bacteria ya que era el diluyente de los aceites esenciales; se midió la absorbancia en el tiempo 0 y 24 horas después, cada prueba se realizó por triplicado la concentración inhibitoria mínima (CMI) y se determinó como la concentración más baja de compuestos ensayados que causó una inhibición del crecimiento del 100% en comparación con el control [15]. Para determinar la concentración mínima bactericida (CMB), se sembraron asépticamente en agar alícuotas de la suspensión bacteriana (100 µl) que no mostraban turbidez visible; La CMB se consideró como la concentración más baja de aceite esencial que inhibe el crecimiento de colonias visibles en el medio [14], [16].
Análisis estadístico
Para llevar a cabo el análisis del perfil químico encontrado dentro de cada aceite esencial se utilizaron boxplots y la prueba ANOVA para comparar de manera individual la concentración de los compuestos. Posteriormente se realizó un análisis de componentes principales (PCA) para evaluar los posibles compuestos que presentaron una mayor influencia dentro de cada AE. Para realizar los análisis de los datos de inhibición en placa, se utilizaron gráficos de barras y se realizó una prueba ANOVA con una prueba post-hoc de Tukey (p-value < 0,05). Finalmente, para los análisis de los datos de las pruebas de inhibición en medio líquido se utilizaron barras y se realizó una prueba t pareada por cada tratamiento con una corrección de Bonferroni (p-value < 0,05). Todos los datos fueron analizados usando Rstudio v4.4.1 (RStudio team, 2024) y las librerías ggplot2, ggpubr, stats, tidyr, dplyr, tidyverse y svglite. Previo al análisis de todos los grupos de datos se aplicó la prueba de Shapiro-Wilk y Levene para confirmar los supuestos de normalidad [17].
Resultados
Análisis de la composición fisicoquímica de los aceites esenciales
La composición química de los tres aceites esenciales obtenidos se organizó en cuatro grupos de metabolitos: monoterpenos oxigenados (MO), monoterpenos hidrocarburos (MH), sesquiterpenos hidrocarburos (SH) y sesquiterpenos oxigenados (SO). De los 39 compuestos determinados en los tres aceites esenciales, inicialmente se comparó la presencia de sus compuestos de manera univariada estableciendo los porcentajes de abundancia encontrados para cada uno de ellos. Se destaca para el aceite esencial de O. majorana L., la presencia de ocho compuestos como Allo-Aromadendreno (SH), Anisol (MO), cis-b-Ocimeno (MH), Germacreno A (SH), p-menta-2,4(8)-dieno (MO), Trans b-Terpineol (MO), b-Omiceno E (MH) y δ-Amorfeno (SH), donde se observa la presencia de los tres grupos de metabolitos encontrados en este estudio (MH, MO y SH), enfatizando la alta producción de los compuestos de tipo MO y SH, entre ellos el Anisol con el 8,24 % de abundancia. Para el caso de R. officinalis L., se resalta la presencia de los compuestos exclusivos Canfor (MO) (12,49 %), Trans-piperitol (MO) y ⍺-terpinoleno (MH). Finalmente, en cuanto a T. vulgaris L, sobresale presencia de compuestos como Aromadreno (SH), Geraniol (MO) y Octeno 2Z (ALC) (tres compuestos) (Figura 1).
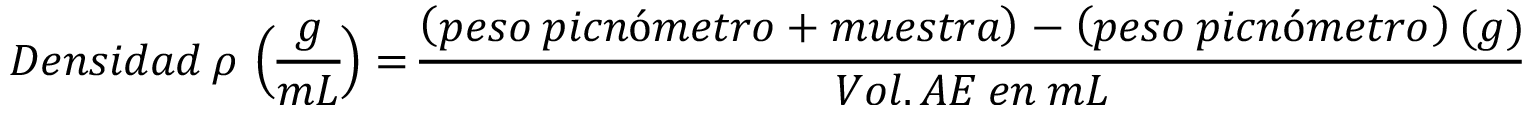
Figura 1. Análisis univariado de las concentraciones de los 39 compuestos encontrados en los aceites esenciales de Origanum majorana (naranja), Rosmarinus officinalis (verde) y Thymus vulgaris (azul).
Se realizó un análisis de componentes principales (PCA) para comparar la composición de los tres aceites esenciales. Inicialmente se observa que cada uno de los aceites evaluados presenta una composición particular, por lo que cada una de las réplicas se agrupa en un cuadrante.
Los resultados muestran que el aceite que presenta mayor influencia, a nivel bioquímico, en su composición es O. majorana; esta planta se encuentra enriquecida con 18 compuestos dentro de los que se resalta un alto contenido de MO (8 compuestos), seguido de SH (6 compuestos) y MH (4 compuestos), cuyos compuestos principales son γ−Terpineno (16,82 %) y trans-Sabineno hidrato (9,57 %). En segundo lugar, se encuentra en el aceite esencial de R. officinalis, con 11 compuestos que corresponden a los más abundantes en el aceite, principalmente del tipo MH (6 compuestos) y MO (5 compuestos) siendo los compuestos principales el a-Pineno (22,48 %) y Eucaliptol (16,62 %). Finalmente, en T. vulgaris los 10 compuestos más abundantes son del tipo MH (6 compuestos), SH (3 compuestos) y un compuesto de tipo alcano (ALC), entre ellos se destaca el γ−Terpineno (33,47 %) y o-Cimeno (17,22 %). Es posible que la actividad antibacteriana de los aceites esenciales se atribuya a estos compuestos que están presentes en mayor abundancia (Figura 2).
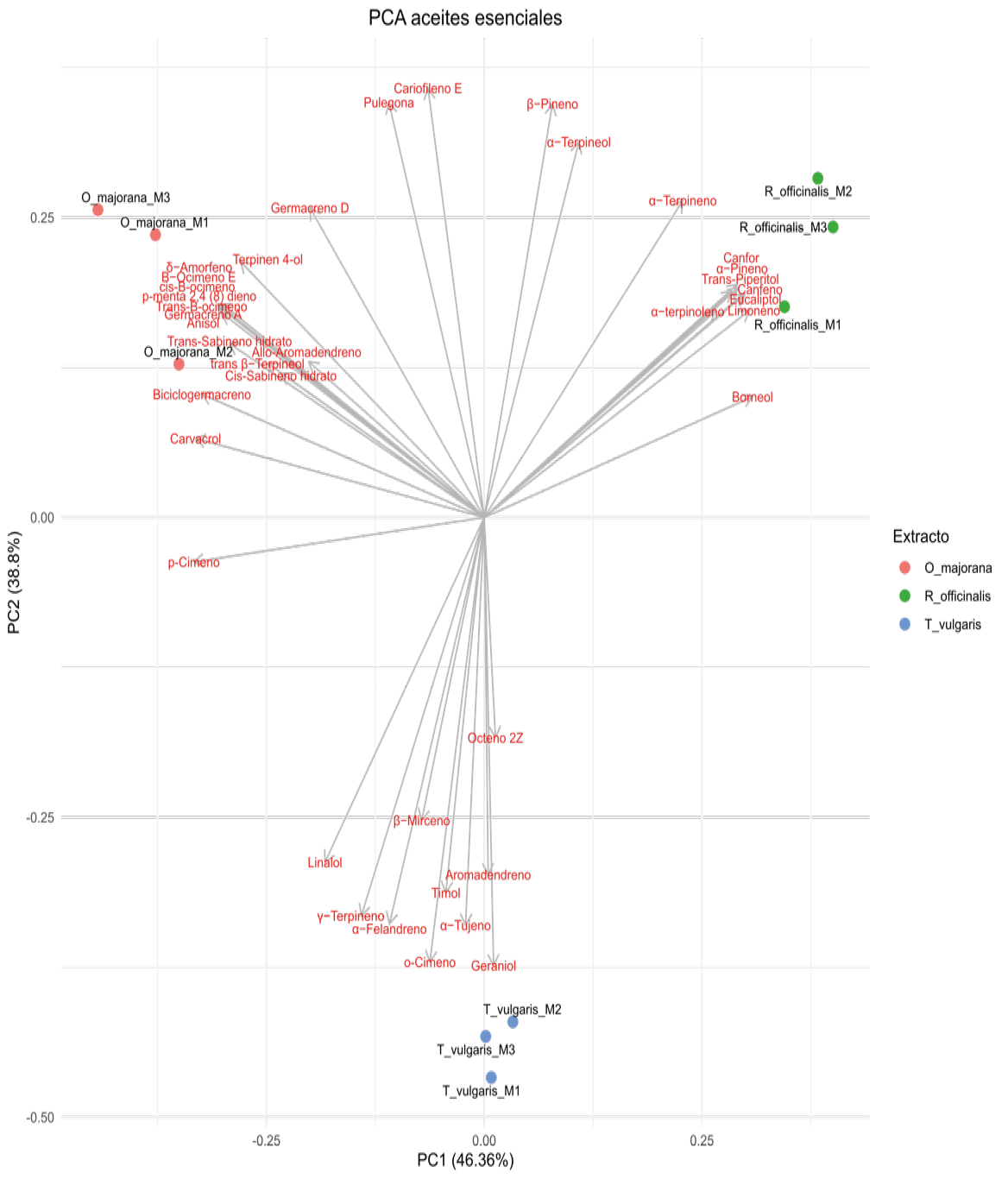
Figura 2. Análisis de componentes principales de la composición de aceites esenciales encontrada en las plantas O. majorana (naranja), R. officinalis (verde) y T. vulgaris (azul).
Para llevar a cabo un análisis que permitiera comparar las variables densidad y rendimiento del aceite esencial con respecto a la biomasa, los resultados permitieron demostrar que no existió una diferencia estadísticamente significativa al comparar la densidad obtenida entre cada uno la cual oscilo entre 0,83-0,87 mg/mL. Sin embargo, se observaron diferencias en los rendimientos; siendo el aceite con el mayor rendimiento el de R. officinalis (0,86 % p/p), seguido del aceite de T. vulgaris (0,31% p/p) y el aceite de O. majorana (0,16 % p/p), los rendimientos encontrados para cada aceite reflejan resultados significativos entre cada uno de ellos Finalmente, se determinó el índice de refracción para O. majorana (1,4877), R officinalis (1,5121) y T. vulgaris (1,4882) (Figura 3).
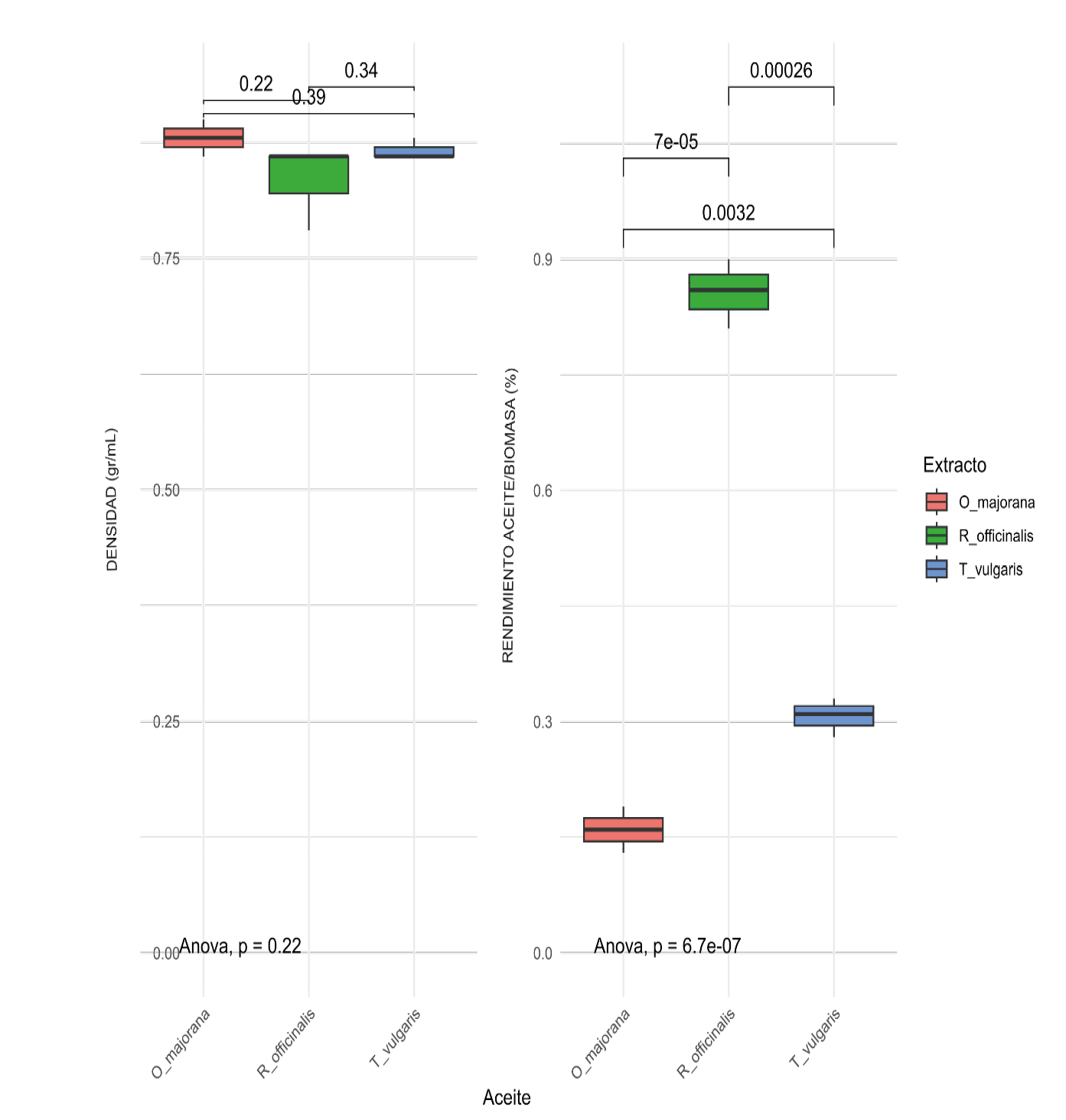
Figura 3. Análisis de densidad (mg/mL) y rendimiento aceite esencial/biomasa (% p/p) para los aceites esenciales encontrados en las especies O. majorana (naranja), R. officinalis (verde) y T. vulgaris (azul). En la parte superior se encuentra el resultado del t-test con el nivel de significancia (p-value < 0,05) y en la inferior se encuentra el resultado de la prueba ANOVA (p-value < 0,05).
Actividad antimicrobiana de los tres aceites esenciales frente a Ralstonia solanacearum, por el método de difusión en agar
Los aceites esenciales han demostrado tener efecto antimicrobiano contra diferentes microorganismos de interés en fitopatología. Dentro de los resultados encontrados se resalta que todos los tratamientos evaluados mostraron un porcentaje de inhibición significativo al compararlos frente al control negativo, lo que determina que los tres aceites esenciales tienen potencial antimicrobiano contra el patógeno. En cuanto a los tratamientos con mayores efectos inhibitorios, los aceites esenciales extraídos para el género O. mejorana (160 mg/mL) y T. vulgaris (80 mg/mL) mostrarían los resultados de inhibición con mayores porcentajes. En cuanto a los resultados obtenidos para R. officinalis, los datos indicarían que, en altas concentraciones, los aceites esenciales tendrían un efecto menor. Por último, los tratamientos y concentraciones propuestas no tendrían diferencias significativas al comparar con el control positivo, lo que indicaría que su efecto no difiere de lo obtenido con el control positivo (rifampicina), exceptuando el resultado que se obtuvo para la concentración de R. officinalis (180 mg/mL) donde se obtendría un porcentaje de inhibición diferente al control positivo (37 % de inhibición) Figura 4 y Tabla1.
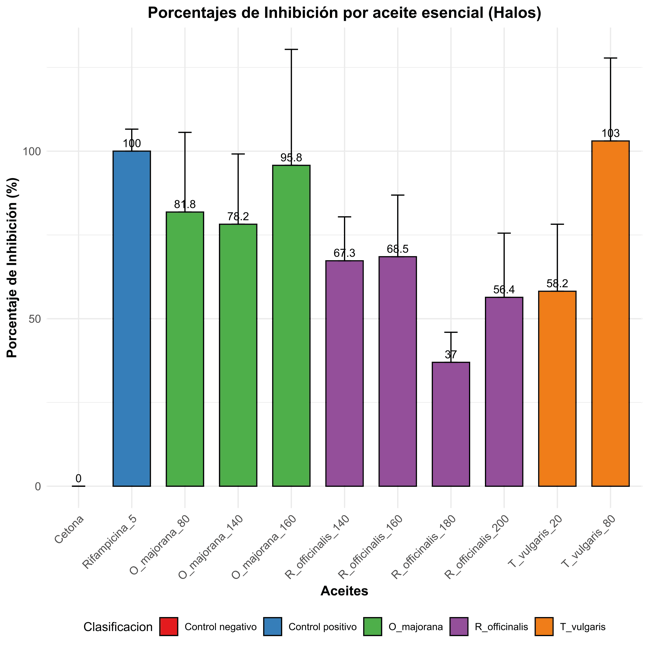
Figura 4 Barplot obtenidos para las pruebas de inhibición en placa de los aceites esenciales obtenidos de O mejorana, R officinalis y T vulgaris en diferentes concentraciones.
Concentración mínima inhibitoria (CMI) y concentración mínima bactericida (CMB)
Se observó que los tratamientos con O. majorana (0,545 mg/mL), R. officinalis (4,37 mg/mL) y T. vulgaris (0,625 mg/mL) presentan inhibición frente a R. solanacearum comparable con el control positivo (rifampicina) al cabo de 24 horas. En algunos casos, el aumento en la concentración de algunos de los aceites puede llevar a un aumento de O.D., sin necesariamente implicar una disminución de la actividad bactericida o antimicrobiana, principalmente por la influencia que pueden presentar factores como la absorbancia del aceite o el medio. Estas concentraciones mantienen un umbral de 12 UFC o menos en todos los tratamientos realizados. Menores concentraciones de aceite en medio liquido podrían llevar al aumento de UFC. Finalmente, los tres aceites esenciales evaluados, son altamente eficientes para la inhibición de crecimiento bacteriano de bacterias como Ralstonia solanacearum, demostrando el alto potencial que tienen para inhibir el crecimiento de patógenos tras su aplicación a nivel agrícola (Figura 5), obteniéndose las CMI y CMB para cada uno de los aceites esenciales presentadas en el cuadro 1.
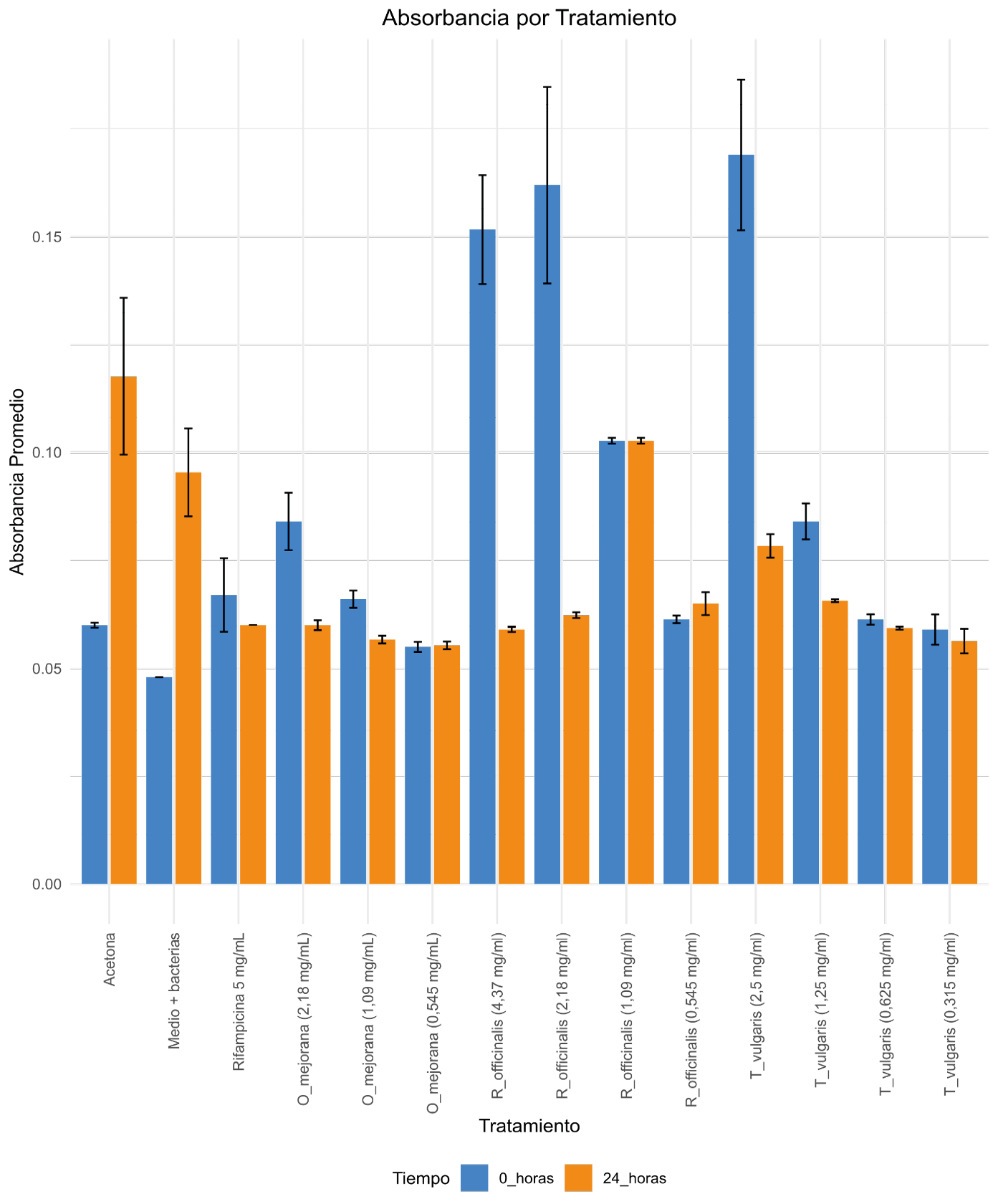
Figura 5. Gráfico de barras de la absorbancia obtenida a las 0 horas y 24 horas para la evaluación del crecimiento de Ralstonia solanacearum en medio liquido durante la interacción con los tres aceites esenciales en diferentes concentraciones.
Cuadro 1. Concentración mínima inhibitoria (CMI) y concentración mínima bactericida (CMB) para cada aceite esencial evaluado frente a Ralstonia solanacearum.
|
Aceite Esencial |
CMI (mg/L) |
CMB (mg/mL) |
|---|---|---|
|
O. majorana L. |
0,545 mg/mL |
1,09 mg/Ml |
|
R. officinalis L. |
1,09 mg/mL |
2,18 mg/mL |
|
T. vulgaris L. |
0,625 mg/mL |
1,25 mg/mL |
Los anteriores resultados permiten demostrar que los aceites esenciales O. majorana, R. officinalis y T. vulgaris tienen efecto antimicrobiano contra el fitopatógeno R. solanacearum en diversas concentraciones.
Discusión y conclusiones
Los aceites esenciales son una mezcla de compuestos que pueden ser extraídos por diferentes métodos, entre los más utilizados se encuentra la hidrodestilación y la destilación por arrastre por vapor, influyendo estos en el rendimiento aceite esencial/biomasa que se pueda obtener. A los aceites esenciales se les han identificado diferentes actividades incluyendo la antimicrobiana, pero su acción depende de la mezcla y cantidad de compuestos, atribuyéndose dicha actividad a la sinergia de sus componentes. Los aceites esenciales pueden representar una alternativa para disminuir o erradicar el uso de plaguicidas químicos sintéticos que generan tanto daño en la cadena trófica y se biodegradan lentamente en el medio ambiente, además, de la producción de compuestos secundarios que pueden ser mucho más tóxicos que los originales, por tal razón es necesario realizar estudios in vitro para determinar si los aceites esenciales funcionan contra diferentes microorganismos que producen enfermedades a nivel de humanos, animales, plantas y proponer una biosolución amigable con el medio ambiente.
Por lo anterior ese necesario conocer las características fisicoquímicas de cada aceite esencial y compararlas con las de otros aceites esenciales obtenidos de la misma especie. Por ejemplo, Mehanna y colaboradores (2022), determinaron para O. majorana L. un rendimiento del 1,1 % p/p, densidad 0,9350 g/mL-0,9430 g/mL e índice de refracción 1,500-1,530, estos valores son superiores a los del presente estudio (0,16 % p/p, 0,87 mg/mL y 1,487, respectivamente). Según los estándares de la farmacopea europea para el aceite de R. officinalis L., el índice de refracción oscila entre 1,464 - 1,473, en el presente estudio el valor fue 1,5121; mientras que para la densidad y el rendimiento se obtuvieron valores dentro del rango establecido. Lugo y colaboradores (2019), para T. vulgaris L. encontraron los valores de densidad (0,934 mg/mL) y del índice de refracción (1,559) superiores los obtenidos en el presente estudio (0,86 mg/mL y 1,482, respectivamente); mientras que el rendimiento se encontró en el mismo 0,15 - 0,57 % p/p. Es importante destacar que el rendimiento al igual que la composición química de los aceites esenciales, depende de diversos factores tales como el método de extracción ya que puede incidir en la obtención de mayor o menor cantidad de aceite, el cultivo, las condiciones edafológicas, geográficas, los periodos de recolección, la altitud, la radiación solar, entre otros [18], [19], [20], [21], [22].
Comparando los resultados de composición química y actividad antimicrobiana de los tres aceites esenciales estudiados, Della y colaboradores (2019) evaluaron el aceite de O. majorana contra bacterias de interés agrícola como P. syringae pv. phaseolica, Xanthomonas campestris, Clavibacter michinganensis, los cuales ejercieron actividad antimicrobiana en concentraciones de 12 mg/mL y 6 mg/ mL con porcentajes de inhibición entre el 20 al 60%, en estos aceites e identificaron principalmente Terpinen-4-ol (29,6 %) y d-2-Careno (20 %), que no se detectaron en nuestro aceite esencial [8]. Mohammed y su grupo de colaboradores determinó para R. officinalis que produjo halos de inhibición entre 8 - 10 mm para diversas bacterias (S. aureus, K. pneumoniae, P. vulgaris), identificando en el aceite esencial 1,8-cineol (17 %) y a-pineno (16,9 %) [6]which endanger antibiotic efficacy. The essential oil of some plants have antimicrobial activity without enhancing the antibiotic resistance.\nMethods: In this study, Rosmarinus officinalis L. from Marivan (Kurdistan Province, Iran. Gedikoğlu y colaboradores (2019 para T. vulgaris determinaron como compuesto principal el timol (51 %), seguido de p-Cimeno (11 %), este último se detectó en el presente trabajo; la acción antimicrobiana se presentó contra bacterias patógenas de interés humano produciendo halos de inhibición entre 13 - 31 mm de diámetro (E. coli, S. typhimurium) sin especificar concentraciones de los aceites [5].
R. solanacearum es un fitopatógeno que ha generado gran preocupación a nivel agrícola por ser cosmopolita y generar grandes pérdidas económicas poniendo en riesgo la seguridad alimentaria, a pesar de que el control químico reduce este tipo de microorganismos a largo plazo producen consecuencias ambientales y metabólicas ya que los microorganismos diana de estas sustancias modifican sus rutas metabólicas para evadir la forma de acción, agravando la situación de los químicos sintéticos. El modo de acción de los aceites esenciales contra R. solanacearum es atribuido a compuestos fenólicos y terpenoides como en los trabajos donde se utilizan aceites esenciales de palmarosa, limoncillo, clavo, eucalipto, Ocimum gratissium, Coriandrum savitum. Hosseini y colaboradores demostraron que el aceites esenciales de Thymus vulgaris generaba inhibición de crecimiento contra R. solanacearum desde 6,5 hasta 35 mm en concentraciones ascendentes desde 0,5 % hasta 100 % y CMI y CMB (1 mg/ml); y de 6,5 a 11 mm (25 – 100 %), CMI (250 mg/ml) y CMB (500 mg/ml) para Rosmarinus officinalis [23]. Hosseinzadeh también trabajo con T. vulgaris cuyo componente mayoritario era el timol y determino una CMB (1,15 ppm) para R. solanacearum [24]. Tanto los datos obtenidos en el presente trabajo como en trabajos similares permiten determinar que la función de los aceites esenciales es la alteración de la membrana por fraccionamiento de lípidos y daño mitocondrial, haciendo estos órganos permeables, causando la salida de moléculas y iones importantes para la bacteria; también se documenta la inhibición de la producción de enzimas como la amilasa y proteasa lo que detiene la producción de toxinas [25]. Es importante mencionar que la diferencia en las concentraciones de los aceites esenciales para la técnica difusión en agar y CMI, CMB, se debe al tipo de soporte líquido y sólido donde esta se desarrolla.
Como conclusión se puede determinar que gracias a la gran variedad de compuestos que poseen los aceites esenciales que han sido ampliamente probados como antimicrobianos contra diversos microorganismos patógenos es posible asegurar que su uso podría reemplazar a los plaguicidas convencionales o por lo menos disminuirlos ya que causan un gran daño a la salud humana, animal y el medio ambiente; los datos de la presente investigación prueban que no todos los aceites esenciales funcionan de la misma manera contra Ralstonia solanacearum tanto en la técnica de difusión en agar como hallando la CMI y CMB. La familia Lamiaceae y los aceites esenciales probados en la presente investigación tienen gran potencial como bioplaguicidas.
Agradecimientos
Facultad de ciencias de la salud de la Universidad Colegio Mayor de Cundinamarca; Dr. Luis Enrique Cuca Suárez Laboratorio de productos naturales y vegetales UNAL, a Magda Roció Gómez Marroquín y el equipo del Centro de investigación Tibaitatá AGROSAVIA (Mosquera-Colombia).
Referencias
[1] F. Vailleau y S. Genin, «Ralstonia solanacearum: an arsenal of virulence strategies and prospects for resistance», Annu. Rev. Phytopathol., vol. 61, n.o 1, pp. 25-47, sep. 2023, doi: 10.1146/annurev-phyto-021622-104551.
[2] A. Abdurahman et al., «Molecular epidemiology of Ralstonia solanacearum species complex strains causing bacterial wilt of potato in Uganda», Phytopathology®, vol. 109, n.o 11, pp. 1922-1931, nov. 2019, doi: 10.1094/PHYTO-12-18-0476-R.
[3] L. R. Ramos da Silva et al., «Lamiaceae essential oils, phytochemical profile, antioxidant, and biological activities», Evidence-Based Complementary and Alternative Medicine, vol. 2021, pp. 1-18, dic. 2021, doi: 10.1155/2021/6748052.
[4] T. M. Karpiński, «Essential oils of Lamiaceae family plants as antifungals», Biomolecules, vol. 10, n.o 1, p. 103, ene. 2020, doi: 10.3390/biom10010103.
[5] A. Gedikoğlu, M. Sökmen, y A. Çivit, «Evaluation of Thymus vulgaris and Thymbra spicata essential oils and plant extracts for chemical composition, antioxidant, and antimicrobial properties», Food Sci Nutr, vol. 7, n.o 5, Art. n.o 5, may 2019, doi: 10.1002/fsn3.1007.
[6] J. J. M. J. Al Zuhairi, F. Jookar Kashi, A. Rahimi-Moghaddam, y M. Yazdani, «Antioxidant, cytotoxic and antibacterial activity of Rosmarinus officinalis L. essential oil against bacteria isolated from urinary tract infection», European Journal of Integrative Medicine, vol. 38, p. 101192, sep. 2020, doi: 10.1016/j.eujim.2020.101192.
[7] S. Nardoni, B. Najar, B. Fronte, L. Pistelli, y F. Mancianti, «In vitro activity of essential oils against Saprolegnia parasitica», Molecules, vol. 24, n.o 7, Art. n.o 7, ene. 2019, doi: 10.3390/molecules24071270.
[8] T. Della Pepa et al., «Antimicrobial and Phytotoxic Activity of Origanum heracleoticum and O. majorana Essential Oils Growing in Cilento (Southern Italy)», Molecules, vol. 24, n.o 14, Art. n.o 14, jul. 2019, doi: 10.3390/molecules24142576.
[9] C. Granados, X. Yáñez, y D. Acevedo, «Evaluación de la actividad antioxidante del aceite esencial Myrcianthes leucoxyla de Norte de Santander (Colombia)», Inf. tecnol., vol. 25, n.o 3, Art. n.o 3, 2014, doi: 10.4067/S0718-07642014000300003.
[10] AOAC, Official methods of analysis, 15.a ed., vol. 1, 5 vols. Washington, DC: AOAC Inc, 1995. Accedido: 12 de septiembre de 2020. [En línea]. Disponible en: https://law.resource.org/pub/us/cfr/ibr/002/aoac.methods.1.1990.pdf
[11] R. Adams, Identification of essential oils components by Gas Chromatography/mass spectrometry, 4th edition., vol. 1. Carol Stream Illinois: Allured Pub Corp, 2007.
[12] C. D. Vargas Baquero, «Bacterias ácido lácticas como biocontroladoras de la marchitez vascular ocasionada por Fusarium oxysporum y Ralstonia solanacearum en tomate», Tesis Maestría, Universidad Nacional de Colombia, Bogotá- Colombia, 2020.
[13] A. Cruz-Carrillo, N. Rodriguez, y Rodriguez Carlos Eduardo, «Evaluación in vitro del efecto antibacteriano de los extractos de Bidens pilosa, Lantana camara, Schinus molle y Silybum marianum», Rev. U.D.CA Act. & Div. Cient., vol. 13, n.o 2, Art. n.o 2, 2010.
[14] L. E. Ramírez y D. Marín Castaño, «Metodologías para evaluar in vitro la actividad antibacteriana de compuestos de origen vegetal», Scientia et technica, vol. XV, n.o 42, Art. n.o 42, 2009.
[15] M. Balouiri, M. Sadiki, y S. K. Ibnsouda, «Methods for in vitro evaluating antimicrobial activity: A review», Journal of Pharmaceutical Analysis, vol. 6, n.o 2, pp. 71-79, abr. 2016, doi: 10.1016/j.jpha.2015.11.005.
[16] L. Orzali, M. T. Valente, V. Scala, S. Loreti, y N. Pucci, «Antibacterial activity of essential oils and Trametes versicolor extract against Clavibacter michiganensis subsp. michiganensis and Ralstonia solanacearum for Seed treatment and development of a rapid in vivo assay», Antibiotics, vol. 9, n.o 9, Art. n.o 9, sep. 2020, doi: 10.3390/antibiotics9090628.
[17] RStudio team. (2024). [En línea]. Disponible en: http://www.posit.co/
[18] T. H. Barak, E. Bölükbaş, y H. Bardakci, «Evaluation of Marketed Rosemary Essential Oils (Rosmarinus officinalis L.) in Terms of European Pharmacopoeia 10.0 Criteria», tjps, vol. 20, n.o 4, pp. 253-260, ago. 2023, doi: 10.4274/tjps.galenos.2022.78010.
[19] L. Lugo-Estrada, S. Galindo-Rodríguez, L. Pérez-López, N. De Torres, y R. Álvarez-Román, «Headspace–solid-phase microextraction gas chromatography method to quantify Thymus vulgaris essential oil in polymeric nanoparticles», Phcog Mag, vol. 15, n.o 63, p. 473, 2019, doi: 10.4103/pm.pm_277_18.
[20] S. Mehanna, M. Y. Issa, N. H. Hassan, A. M. Hussien, M. A. Ibrahim, y E. I. Hassanen, «Origanum majorana essential oil improves the rat’s sexual behavior and testicular oxidative damage induced by imidacloprid via modulating the steroidogenesis pathways», Saudi Pharmaceutical Journal, vol. 30, n.o 9, pp. 1315-1326, sep. 2022, doi: 10.1016/j.jsps.2022.06.016.
[21] M. Chetouani, R. Chetouani, E. Loukili, y B. Hammouti, «The qualitative and quantitative study of Rosmarinus officinalis essential oils under the effect of water stress at the juvenile and adult stages in greenhouse», J. Mater. Environ. Sci., vol. 14, n.o 8, pp. 967-977, 2023.
[22] A. Raffo et al., «Effect of Different Soil Treatments on Production and Chemical Composition of Essential Oils Extracted from Foeniculum vulgare Mill., Origanum vulgare L. and Thymus vulgaris L.», Plants, vol. 12, n.o 15, p. 2835, jul. 2023, doi: 10.3390/plants12152835.
[23] M. Hosseini Nezhad, L. Alamshahi, y N. Panjehkeh, «Biocontrol efficiency of medicinal plants against Pectobacterium carotovorum, Ralstonia solanacearum and Escherichia coli», TOPROCJ, vol. 3, n.o 1, pp. 46-51, nov. 2012, doi: 10.2174/1876326X01203020046.
[24] S. Hosseinzadeh, M. Shams-Bakhsh, y E. Hosseinzadeh, «Effects of sub-bactericidal concentration of plant essential oils on pathogenicity factors of Ralstonia solanacearum», Archives of phytopathology and plant protection, vol. 46, n.o 6, pp. 643-655, abr. 2013, doi: 10.1080/03235408.2012.749698.
[25] B. R. Ghalem, «Essential Oils as Antimicrobial Agents Against Some Important Plant Pathogenic Bacteria and Fungi», en Plant-Microbe Interaction: An Approach to Sustainable Agriculture, D. K. Choudhary, A. Varma, y N. Tuteja, Eds., Singapore: Springer Singapore, 2016, pp. 271-296. doi: 10.1007/978-981-10-2854-0_13.
Declaración sobre uso de Inteligencia Artificial (IA)
Los autores aquí firmantes declaramos que no se utilizó ninguna herramienta de IA para la conceptualización, traducción o redacción de este artículo.
1 Universidad Colegio Mayor de Cundinamarca Bogotá-Colombia.
 jacerog@unicolmayor.edu.co
jacerog@unicolmayor.edu.co https://orcid.org/0000-0003-1656-6888
https://orcid.org/0000-0003-1656-68882 Instituto Tecnológico de Costa Rica. Cartago, Costa Rica.
 tjguzman@itcr.ac.cr
tjguzman@itcr.ac.cr https://orcid.org/0000-0002-2719-8550
https://orcid.org/0000-0002-2719-85503 Universidad Nacional de Colombia.
 wadelgadoa@unal.edu.co
wadelgadoa@unal.edu.co https://orcid.org/0000-0001-8415-7950
https://orcid.org/0000-0001-8415-79504 Universidad Nacional de Colombia, Sede Bogotá, Colombia.
 jalcantara@unal.edu.co
jalcantara@unal.edu.co https://orcid.org/0000-0003-1176-2599
https://orcid.org/0000-0003-1176-25995 AGROSAVIA.
 msoto@agrosavia.co
msoto@agrosavia.co https://orcid.org/0000-0002-2392-2839
https://orcid.org/0000-0002-2392-2839 6 Pontificia Universidad Javeriana. Colombia.
 egil@javeriana.edu.co
egil@javeriana.edu.co https://orcid.org/0000-0002-1774-970X
https://orcid.org/0000-0002-1774-970X