Resonancia Magnética Nuclear en Costa Rica: una perspectiva histórica
Nuclear Magnetic Resonance in Costa Rica: a historical perspective
José Andrés Borloz-Chinchilla1, Isaac F. Céspedes-Camacho2
Fecha de recepción: 31 de agosto, 2023
Fecha de aprobación: 9 de diciembre, 2023
Borloz-Chinchilla, J.A; Céspedes-Camacho, I.F. Resonancia Magnética Nuclear en Costa Rica: una perspectiva histórica. Tecnología en Marcha. Vol. 37, No 3. Julio-Setiembre, 2024. Pág. 48-76. https://doi.org/10.18845/tm.v37i2.6870
https://doi.org/10.18845/tm.v37i2.6870
Palabras clave
Resonancia magnética nuclear; historia de la ciencia; espectroscopía; campos magnéticos; artículo de revisión.
Resumen
La Resonancia Magnética Nuclear (RMN) es una técnica ampliamente utilizada para la elucidación y caracterización estructural de moléculas orgánicas gracias a la interacción de la materia con un campo magnético. Desde la adquisición del primer equipo de RMN en Costa Rica, a finales de la década de los 70’s, la ciencia costarricense en general y la química en particular, dieron un salto significativo, generando investigaciones de impacto y una gran cantidad de publicaciones y trabajos de graduación. Por primera vez en la historia de la ciencia costarricense se presenta un estudio detallado del desarrollo de la RMN en el país, gracias a una revisión exhaustiva de fuentes primarias y secundarias. El presente documento muestra una recopilación histórica de los equipos de RMN con que ha contado el país, los resultados obtenidos con ellos y una perspectiva histórica sobre su uso en el pasado y a futuro.
Keywords
Nuclear Magnetic Resonance; history of science; spectroscopy; magnetic fields; review.
Abstract
Nuclear Magnetic Resonance (NMR) is a widely used technique for the elucidation and structural characterization of organic molecules thanks to the interaction of matter with a magnetic field. Since the acquisition of the first NMR in Costa Rica, at the end of the 70s, Costa Rican science in general, and chemistry in particular, have taken a significant step, by generating impact research and many publications and theses. For the first time in the history of Costa Rican science, a detailed study of the development of NMR in the country is presented, thanks to an exhaustive review of primary and secondary sources. This document shows a historical compilation of the NMR equipment presented in the country, the results obtained with them and a historical perspective about its use.
Introducción
La Resonancia Magnética Nuclear (RMN) es una técnica que fue descubierta por los físicos Edward M. Purcell de la Universidad de Harvard y Félix Bloch de la Universidad de Stanford durante la década de los 40’s, quienes observaron el fenómeno de forma simultánea, aunque independientemente. Dicho descubrimiento les valió el Premio Nobel de Física de 1952 [1]. Cinco premios Nobel han sido otorgados, hasta la fecha, a científicos que han realizado aportes significativos a la RMN, lo que demuestra la enorme importancia de esta técnica.
La RMN basa su funcionamiento en el aprovechamiento de la abundancia natural de ciertos isótopos (con un número cuántico de espín nuclear S, distinto de cero), tales como el 1H, 13C, 15N o 19F, para mencionar los más comunes [2, 3]. Cuando a los núcleos de estos isótopos se les aplica un campo magnético externo B0, estos adquieren orientaciones respecto a él, dependiendo de sus niveles energéticos [4, 5]. Los núcleos comienzan a realizar un movimiento de precesión, similar al de un trompo, a una determinada frecuencia, la llamada frecuencia de Larmor g [6]. El fenómeno de la RMN ocurre cuando los núcleos orientados respecto a B0 son inducidos a absorber energía a partir de una onda de radiofrecuencia externa, emitida como un pulso (i.e., una onda de alta intensidad y de corta duración), cuya frecuencia debe corresponder directamente con la g del núcleo de interés, produciendo un cambio en las poblaciones de los espines [2]. Al finalizar el pulso, las poblaciones de espines vuelven a sus estados originales, a través de un proceso de relajación, que se detecta como una onda de decaimiento de inducción libre (FID, por sus siglas en inglés) [7]. Con ayuda de una transformada de Fourier, el FID se convierte al dominio de la frecuencia, generando el espectro final de RMN.
A partir de dicho espectro, la RMN es empleada en el estudio de propiedades físicas, químicas y biológicas de la materia. Posee gran cantidad de aplicaciones en ciencia y tecnología, por ejemplo, para la determinación de la pureza de una muestra [8–16], desarrollo de análisis no destructivos [17–24], elucidación estructural de compuestos químicos [25–33], metabolómica [34–39], estudios relacionados a la dinámica molecular [40–47] o en el análisis de proteínas [48–53]. La RMN ha evolucionado de forma significativa, permitiendo el análisis tanto de sustancias líquidas como sólidas [54, 55]. Además, dependiendo del régimen de magnitud del campo magnético utilizado, puede clasificarse como de campo alto (high-field) o de campo bajo (low-field). Inclusive, en los últimos años, han sido desarrolladas líneas de investigación utilizando la RMN con campos magnéticos tan bajos como el campo magnético terrestre (i.e. entre 50 y 100 mT [2, 56, 57]), pretendiendo alcanzar condiciones biológicas que permitan obtener una mayor comprensión de diversos fenómenos naturales [57–61].
Esta técnica es una herramienta indispensable para las ciencias naturales, en general, y para la química en particular. Su uso en investigación es innegable y brinda información que con otras técnicas espectroscópicas sería imposible obtener. Actualmente, Costa Rica cuenta con tres equipos de RMN, dos de campo alto (400 MHz y 600 MHz) en la Escuela de Química y en el Centro de Investigación en Productos Naturales (CIPRONA), ambos en la Universidad de Costa Rica (UCR) y uno de campo bajo (60 MHz) en la Escuela de Química del Tecnológico de Costa Rica (TEC). Estos equipos se han utilizado mayoritariamente en la caracterización estructural y elucidación de compuestos orgánicos, aunque en los últimos años se han realizado avances importantes en la RMN de sólidos y la RMN en régimen de campo bajo [62].
A pesar de que esta técnica ha existido en Costa Rica desde hace casi 50 años, hasta la fecha no se llevado a cabo ningún estudio bibliográfico a nivel nacional que presente los inicios, desarrollo y principales aplicaciones de la RMN en el país. Por lo tanto, el presente artículo de revisión pretende subsanar esta situación mostrando, en primer lugar, y para tener un contexto histórico, el desarrollo de la RMN a nivel mundial. Posteriormente, mediante un recopilatorio bibliográfico exhaustivo basado en fuentes primarias y secundarias, mostrar el desarrollo de la técnica desde sus inicios y hasta la fecha, en Costa Rica. Además, con la ayuda de este respaldo bibliográfico y apoyados en estudios recientes, se ofrece una perspectiva sobre cómo puede utilizarse la RMN en sus distintas áreas, para mejorar los índices de investigación, desarrollo e innovación en Costa Rica.
Perspectiva Histórica de la RMN
Previo al descubrimiento de la RMN como tal, se llevaron a cabo distintos estudios sobre la relación entre el campo magnético y los núcleos atómicos. Isdor Isaac Rabi sometió muestras de sólidos cristalinos a campos magnéticos y rayos moleculares de compuestos iónicos (i.e. LiCl), con lo que logró calcular el momento magnético de los protones, que a su vez conllevó a la deducción y posterior comprobación del momento magnético del neutrón, registrando así las propiedades magnéticas del núcleo atómico [1, 63–65]. Estos descubrimientos le valieron el Premio Nobel de Física en el año 1944. Fue Rabi quien fundamentó las bases que servirían para el posterior descubrimiento de la RMN. Previo a él, Otto Stern, también ganador del Nobel de Física en 1943, determinó el momento magnético del protón [65, 66].
Como mencionado anteriormente, la técnica de RMN fue descubierta por primera vez de forma simultánea, pero independientemente, por los físicos Edward M. Purcell de la Universidad de Harvard y Félix Bloch de la Universidad de Stanford (quien dio nombre a la técnica, pues previamente era conocida como inducción nuclear) aproximadamente a inicios de 1946 [1, 65, 67, 68]; descubrimiento que les valió el Premio Nobel de Física de 1952. Posterior a dicho descubrimiento, en el año 1951, Arnold Dharmatti y Martin Packard, ambos en la Universidad de Stanford, emplearon la técnica recién descubierta en una muestra de etanol, lo que los llevó a observar tres tipos de señales, cada una correspondiente a los distintos tipos de protones de hidrógeno presentes en la molécula de etanol que, al ser analizadas a profundidad, les permitieron determinar la relevancia de la presente técnica en posibles análisis espectroscópicos [69].
De la misma forma, tal y como se indica en [1], se desarrollaron métodos de estudio en sistemas y muestras sólidas, dando nacimiento a la RMN de estado sólido. En 1948 se hizo la primera observación de una señal definida de la interacción dipolo-dipolo de moléculas de agua cristalizada en una disolución [70]. La RMN de estado sólido presentaba problemas en la resolución de los espectros obtenidos, lo que obligó al desarrollo de técnicas como el Magic Angle Spinning (MAS) [71], que inclina la muestra a un ángulo de 54,7° aproximadamente respecto al campo magnético aplicado, eliminando ciertas interferencias anisotrópicas [72].
Los primeros equipos de RMN comercializados tenían una magnitud de radiofrecuencia de 60 MHz, que, debido a diversos problemas (e.g. superposición en las señales y alta inestabilidad), fueron gradualmente actualizados y mejorados mediante distintas técnicas. Estos primeros equipos funcionaban a partir de barridos de onda continua, en los que se analizaba poco a poco las frecuencias a las que se detectaban señales de resonancia, sin embargo, esta técnica resultaba ineficiente [4].
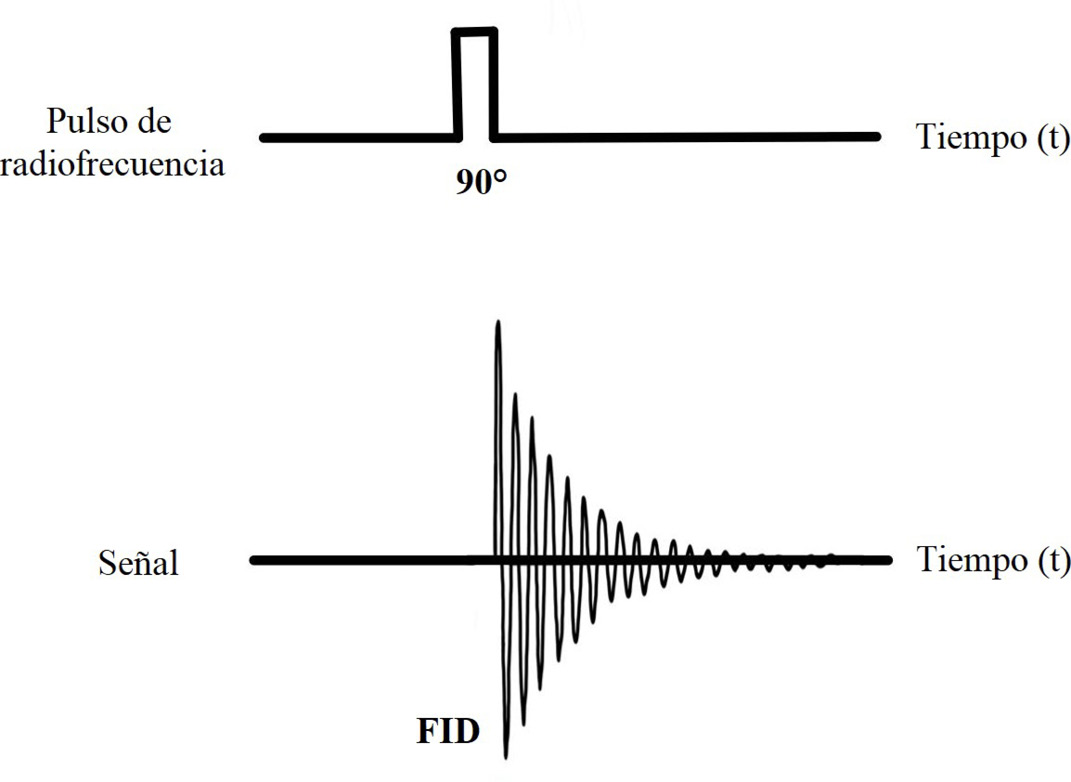
Figura 1. Pulso de radiofrecuencia y FID consiguiente. Adaptado de [74].
A mediados de los 60’s, Richard Ernst y Weston Anderson, a partir de métodos matemáticos, iniciaron el desarrollo del método de pulsos, que simplificó el análisis de la técnica y eliminó los barridos de onda continua. Este procedimiento, a través de los fenómenos de relajación, produce el FID; el cual es analizado mediante el uso de la transformada de Fourier [73]. En la figura 1 se muestra la relación entre el pulso producido por la onda de radiofrecuencia y la señal de FID generada por la relajación de los espines.
Los instrumentos que funcionaban a partir de la transformada de Fourier y de la emisión de pulsos de radiofrecuencia implicaron un importante avance respecto a la metodología utilizada a la hora de hacer mediciones de RMN.
En la década de los 70’s, Richard Ernst fue capaz de desarrollar una técnica que le permitía obtener espectros en dos dimensiones [75]; descubrimiento por el que fue laureado con el Premio Nobel de Química en el año 1991. Dicha técnica hace posible el análisis de moléculas complejas, sirviendo como punto de partida para el desarrollo de las Imágenes por Resonancia Magnética (MRI, por sus siglas en inglés) [1], aplicada en diagnósticos e imágenes médicas.
Asimismo, Kurt Wüthrich fue galardonado en el año 2002 con el Premio Nobel de Química, gracias a sus aportes en el desarrollo de la espectroscopia de RMN para la determinación de la estructura tridimensional de macromoléculas [1, 76], convirtiendo a la RMN en una de las técnicas más laureadas de los últimos años. Esto no quiere decir que esta técnica se haya estancado, por el contrario, los avances de los últimos años son significativos [77, 78], con desarrollos de imanes cada vez más potentes, los cuales permiten el estudio de sistemas más complejos, con una alta resolución (i.e. high-field NMR, por su nombre en inglés). Paralelo a estos avances se ha propiciado ampliamente el desarrollo de la técnica con imanes permanentes que, aunque de más baja resolución por su B0 más bajo, brindan una mayor accesibilidad a la técnica a través de los RMN de escritorio [79–84]. Incluso, se están realizando estudios en el campo magnético terrestre y hasta en B0 ≈ 0 (i.e. Earth and Zero Field NMR) [85]. Por otro lado, el desarrollo de fenómenos de hiperpolarización ha ayudado a mejorar la inherente baja sensibilidad de la RMN [86, 87]. Los avances en el campo de la RMN no han parado, y aún queda mucho por investigar.
RMN en Costa Rica
La RMN ha sido una técnica clave para el desarrollo científico y tecnológico del país. Se han realizado avances en distintas áreas del conocimiento, principalmente en la caracterización estructural y la elucidación de compuestos químicos. Actualmente, se cuenta con tres equipos de RMN en funcionamiento en el país, dos de los cuales pertenecen a la UCR y uno al TEC. Esta sección muestra el desarrollo de la RMN en el país, a partir de una descripción general de todos los equipos de RMN que se han instalado y utilizado en Costa Rica. Esta información se ha obtenido gracias, principalmente, a entrevistas con investigadores que trabajaron o fueron parte del proceso de adquisición, instalación y manejo de los equipos descritos.
A. Equipos de RMN en el país
A continuación, se presenta una revisión histórica de todos los equipos de RMN registrados en el país, partiendo del más antiguo, hasta los más modernos, para así tener una visión lineal del desarrollo de la técnica.
A.1. Primer Equipo: Perkin-Elmer R12A (60 MHz)
A finales de la década de los setenta, Costa Rica adquiere su primer equipo de RMN, el cual se instaló en el CIPRONA, dirigido en aquel entonces por el profesor José Guillermo Calzada, correspondiente al modelo R12A de 60 MHz de la marca Perkin-Elmer [88, 89]. Este modelo funcionaba a partir del principio de onda continua, con una sonda de 5 milímetros, calibrado a partir de perillas y con el cual solo era posible medir espectros protónicos. Debido a que funcionaba con onda continua, resultaba muy difícil de calibrar, pero sencillo de operar [90]. Por la naturaleza del dispositivo, los análisis de muestras requerían lapsos de tiempo significativamente largos. Este equipo fue utilizado en la academia, en cursos impartidos en la carrera de Química de la UCR, tanto de forma experimental como teóricamente. Ejemplos de esto fueron los cursos de Química Orgánica Preparativa y Análisis Orgánico [89, 90]. El R12A dejó de utilizarse debido a la inestabilidad de la corriente eléctrica, lo que producía una pérdida parcial o total del campo magnético, lo que implicó altos costos económicos y tiempo. Para 1982 el equipo dejó de funcionar [90]. En la figura 2 se muestra una imagen del equipo R12A de Perkin-Elmer, tomado de una publicidad del mismo.

Figura 2. Imagen del Perkin-Elmer R12A de 60 MHz, primer modelo de RMN adquirido en el país. Tomado de [91].
A.2. Segundo Equipo: Varian EM360 (60 MHz)
Luego de la adquisición del R12A en la UCR, el interés por la técnica de RMN aumentó en el país. Por esta razón, la Universidad Nacional de Costa Rica (UNA) inició gestiones para la adquisición de un equipo de RMN propio, especialmente considerando la necesidad del Departamento de Veterinaria (ubicado en Barreal de Heredia) de dicha universidad en la identificación de principios activos en plantas tóxicas que eran alimento de ganado, temática de un proyecto de investigación vigente en ese momento [88]. En 1982, y gracias a una donación de la Agencia Española de Cooperación, la UNA recibió su primer RMN, el cual era un modelo EM360 de 60 MHz de la marca Varian. Al igual que el R12A, este equipo funcionaba mediante el principio de onda continua [92].
El lugar donde fue instalado presentaba mucha inestabilidad en la red eléctrica, por lo que se requerían bancos de baterías que permitieran el buen funcionamiento del dispositivo sin demasiada inestabilidad. Debido al alto costo en el mantenimiento (i.e. aproximadamente $2000/por mes, de la época), adquisición de criogénicos y disolventes deuterados, así como la inestabilidad eléctrica, propiciaron que el equipo fuera descartado por completo en el año 1986 [88]. En la figura 3 se muestra una fotografía del RMN Varian EM360 instalado en la sede central de la UNA.

Figura 3. Fotografía del Dr. Marco Calvo Pineda junto al RMN Varian EM360 de 60 MHz, ubicado en la UNA. Foto provista por el Dr. Calvo Pineda.
A.3. Tercer equipo: Hitachi & Perkin-Elmer R24-B (60 MHz)
Además de los equipos antes descritos presentes en instituciones de educación superior, el laboratorio de la Dirección General de Aduanas (DGA) de Costa Rica también ha contado con equipos de RMN, los cuales se han utilizado mayoritariamente para la elucidación e identificación de sustancias.
La DGA adquirió el primer equipo de RMN en 1982, con presupuesto propio de la institución, el cual era un modelo R24-B de 60 MHz de las empresas Hitachi y Perkin-Elmer [93, 94]. Al igual que los equipos anteriores, funcionaba bajo el principio de onda continua [89]. Solo hacía mediciones de 1H y tenía la capacidad de hacer desacoplamientos electrónicos. Fue ampliamente utilizado para cuantificación de diversos analitos, así como para la determinación de índices de saponificación, destacando su uso en la prestación de servicios. Su uso en aplicaciones académicas fue más limitado, hasta que el equipo fue dado de baja en el año 2000 [93, 94]. En la figura 4 se muestra un dispositivo R24-B de 60 MHz, similar al del laboratorio de la DGA.

Figura 4. Dispositivo Hitachi & Perkin-Elmer R24-B de 60 MHz. Tomado de [95].
A.4. Cuarto equipo: JEOL JNM-FX90Q (90 MHz)
Para finales del año 1982, el profesor José Guillermo Calzada gestionó la obtención de un nuevo dispositivo de RMN para el país a partir de un convenio con el gobierno japonés [90, 96]. Gracias a este acuerdo, se logró obtener un RMN de la marca JEOL, modelo JNM-FX90Q de 90 MHz, el cual fue ubicado en el CIPRONA. El nuevo equipo brindó un paradigma completamente diferente y novedoso respecto a lo que se tenía hasta la fecha, ya que era el primer equipo que funcionaba por encima de los 60 MHz, además de que su funcionamiento se basaba en el uso de la transformada de Fourier y no mediante el barrido de onda continua previamente descrito. Una fotografía del dispositivo instalado en el CIPRONA se muestra en la figura 5.

Figura 5. JEOL 90 MHz ubicado en el CIPRONA, operado por la Dra. Rosaura Romero. Tomado de [97].
A partir de la experiencia en los equipos de RMN anteriores, para este equipo de 90 MHz se emplearon baterías UPS (Uninterruptible Power Supply, por sus siglas en inglés), además de la alimentación por una planta eléctrica, con el objetivo de procurar una mayor estabilidad del campo magnético generado [90, 96]. Con este equipo se lograron avances significativos pues fue posible realizar experimentos diferentes al 1H, así como experimentos en dos dimensiones, tales como el COSY (Correlation Spectroscopy, por sus siglas en inglés). El JNM-FX90Q se controlaba mediante software y no con perillas como dispositivos anteriores. En sus primeros años, el dispositivo no fue usado ampliamente y se enfocó principalmente en capacitar al personal y en aprender cómo funcionaba esta novedosa tecnología [96].
Al igual que los otros dispositivos, se tenían problemas con la inestabilidad en la electricidad debido a que funcionaban a partir de electroimanes. A este dispositivo se le realizaban labores de mantenimiento continuamente, hasta que, para el año 1995, el dispositivo dejó de funcionar [90].
A.5. Quinto equipo: Varian Mercury 400 Plus (400 MHz)
En 1997, gracias a una donación de la fundación CRUSA (Cooperación Costa Rica - Estados Unidos) se adquirió el primer equipo de campo alto en el país, modelo Mercury 400 Plus de la marca Varian, con una frecuencia de 400 MHz, el cual tuvo un costo de aproximadamente $275 000 [90]. El uso y mantenimiento del equipo se logró gracias a una alianza entre la UCR y el Instituto Nacional de Biodiversidad (InBio), que resultó en la formación de la Unidad de Espectroscopia de Resonancia Magnética Nuclear (UE-RMN), la cual ofrecía servicios especializados y de alto nivel para la industria, la academia, el gobierno y el público [98]. Este equipo se encuentra actualmente en la Escuela de Química de la UCR y contaba inicialmente con un espectrómetro capaz de medir espectros de 1H, 13C, 19F, 31P y cualquier núcleo hasta la frecuencia de resonancia del 15N [98]. Además, con el equipo se pueden realizar una diversidad de experimentos en dos dimensiones.
Una reforma fue hecha en el año 2010, donde fue desenergizado para cambiar los empaques y darle más años de vida. Con la compra del RMN de 600 MHz (vide infra) se gestionó un cambio de tecnología en este dispositivo, pasando a un magneto de la empresa Bruker, por un costo de aproximadamente $100 000 [90]. En la figura 6 se muestra el modelo del Varian Mercury de 400 MHz ubicado en la UCR.

Figura 6. Dispositivo de RMN Varian Mercury 400 Plus de 400 MHz, modelo del ubicado en la UCR. Tomado de [99].
El equipo funciona a partir de un sistema criogénico de nitrógeno y helio líquido, primero en el país, los cuales deben ser reemplazados cada 15 días y una vez al año, respectivamente. Para evitar problemas con las señales generadas por el dispositivo y para preservar la electrónica que lo compone, se le mantiene en un cuarto a temperatura controlada entre 20 y 23 °C [90]. El instrumento está equipado con un accesorio de gradiente de campo y dos sondas para realizar detecciones especializadas (i.e. detección inversa y detección en modo normal) [98].
Al haber sido el primer equipo de campo alto, la resolución de los espectros generados aumentó significativamente, así como la calidad y cantidad de los experimentos realizados [90]. Todo esto se ve reflejado en las aplicaciones desarrolladas en el país desde esa fecha en publicaciones, proyectos de investigación y tesis. Por otro lado, el equipo ha sido utilizado en diversos cursos de grado y postgrado en el país, permitiendo un conocimiento y aprovechamiento de la técnica nunca antes visto.
A.6 Sexto equipo: Anasazi EFT-90 (90 MHz)
En el año 2009, como parte de una donación de la Secretaría de Integración Económica Centroamericana (SIECA), el laboratorio de la DGA recibió un nuevo equipo de RMN de 90 MHz, correspondiente al modelo EFT-90 de la marca Anasazi [100]. El dispositivo funcionaba a partir del principio de transformada de Fourier y mediante un imán permanente de 2,1 T, con la capacidad de hacer mediciones en gran variedad de núcleos, pues el equipo estaba equipado con una sonda de multinúcleos, además de contar con la posibilidad de realizar experimentos en dos dimensiones [101].
En el laboratorio de la DGA se llevaron a cabo múltiples experimentos, principalmente realizando mediciones en aceites comestibles, índices de yodo, peso molecular promedio, análisis de productos químicos orgánicos y de compuestos organofosforados, mediante el uso de los núcleos de 1H, 13C, 15N, 19F, 31P, experimentos DEPT (Distortionless Enhancement by Polarization Transfer, por sus siglas en inglés) así como experimentos en dos dimensiones [100]. El equipo fue ampliamente aprovechado hasta el año 2014, en que dejó de funcionar debido a problemas eléctricos en el equipo [100]. En la figura 7 se muestra el modelo del EFT-90, usado en el laboratorio de la DGA.

Figura 7. Dispositivo de RMN Anasazi EFT-90, de 90 MHz. Modelo del segundo RMN usado en el laboratorio de la DGA. Tomado de [101].
A.7. Séptimo equipo: Bruker Ascend 600 (600 MHz)
En el año 2010, el CIPRONA adquirió un RMN de 600 MHz de la marca Bruker, modelo Ascend 600, el cual tuvo un costo de aproximadamente $850 000. Hasta la fecha es el equipo de más alta resolución funcionando en el país. El mismo se encuentra en las instalaciones del CIPRONA en la Ciudad de la Investigación en la UCR y, al igual que el RMN de 400 MHz, necesita de una habitación con temperatura controlada. Por otro lado, este magneto está aislado (ultra shielded), lo que permite que cualquier operador pueda manejarlo sin ningún problema para su salud. Como este equipo no posee un automuestreador, el operador técnico debe colocar las muestras individualmente [90]. Asimismo, el equipo se maneja con ayuda del software TopSpin, el cual cuenta con una amplia biblioteca de secuencias de pulsos para experimentos en una y dos dimensiones.
Al igual que el Varian Mercury, dicho equipo requiere de sistemas criogénicos y cuenta con 3 canales para el ingreso de sondas [90]. Al ser el equipo con la más alta resolución en el país, es posible realizar análisis de moléculas con alto peso molecular y sistemas complejos, obteniendo información estructural importante incluso en experimentos de 3 dimensiones [102]. El dispositivo de RMN Bruker de 600 MHz ubicado en el CIPRONA, se muestra en la figura 8.

Figura 8. Equipo de RMN Bruker Ascend 600, de 600 MHz, ubicado en el CIPRONA. Tomado de [102].
A.8. Octavo equipo: Magritek Spinsolve 60 (60 MHz)
En los últimos años, el desarrollo de la RMN en campo bajo ha sido significativo, generando resultados prometedores [79–84]. Gracias a este desarrollo, en el año 2022, la Escuela de Química del TEC decidió adquirir un equipo de 60 MHz de la marca Magritek, modelo Spinsolve 60. El equipo se financió con apoyo de la Vicerrectoría de Investigación y Extensión (VIE) por un monto de $60 000 [103]. Se instaló en el Edificio de la Escuela de Química del TEC.
Dicho equipo cuenta con una bomba peristáltica y una sonda de monitoreo para el estudio de la cinética de reacciones químicas en tiempo real [103]. A diferencia de los equipos de campo bajo previamente descritos, el mantenimiento del Spinsolve 60 es prácticamente nulo y cuenta con una interfase amigable con el usuario. No obstante, el magneto permanente es altamente sensible a variaciones en la temperatura. El software de este equipo permite realizar experimentos de 1H, 13C y 19F, además de experimentos en dos dimensiones tales como COSY, NOESY (Nuclear Overhauser Enhancement Spectroscopy, por sus siglas en inglés) y DEPT.
Aunque el equipo cuenta con una baja sensibilidad en comparación con el Bruker de 600 MHz o el Varian Mercury de 400 MHz, los experimentos en este equipo se pueden realizar en ausencia de disolventes deuterados, lo que abarata costos y hace más accesible la técnica a un público más amplio.
Actualmente el equipo se ha utilizado en laboratorios de docencia para el análisis de muestras sencillas. Asimismo, se están desarrollando metodologías para su uso en los centros de investigación del TEC y para brindar servicio a la industria local. Por otro lado, el equipo pretende involucrar estudiantes de distintas disciplinas académicas para el desarrollo de sus tesis y Trabajos Finales de Graduación (TFG). Una fotografía del equipo ubicado en la Escuela de Química del TEC se muestra en la figura 9.

Figura 9. Dispositivo de RMN Spinsolve 60, de la marca Magritek, de 60 MHz, ubicado en la Escuela de Química del TEC.
B. Aportes de la RMN a la docencia y la investigación en Costa Rica
La RMN ha proporcionado un amplio margen para la investigación y el desarrollo científico del país, lo cual se ve reflejado en el extenso número de investigaciones científicas relacionadas a dicha técnica, y cuyos resultados han generado una serie extensa de publicaciones en revistas indexadas, tesis de grado y posgrado, así como presentaciones en eventos nacionales e internacionales.
Luego de una extensa revisión bibliográfica, ha sido posible presentar las principales áreas temáticas en donde la RMN ha sido utilizada, ya sea con los equipos instalados en el país, o bien, en colaboraciones internacionales brindando asesoría y apoyo en la técnica. El cuadro 1 muestra estos resultados, con las citas bibliográficas correspondientes para una búsqueda más expedita por parte del lector.
Cuadro 1. Aplicaciones directas de la técnica de RMN en investigación realizada en Costa Rica o por costarricenses.
|
Aplicación |
Referencias |
|
Elucidación, identificación y caracterización estructural |
[104–225] |
|
Estudio de proteínas |
[226, 227] |
|
Estudio de materiales |
[228–230] |
|
Otros estudios |
[231–245] |
Más de 140 artículos científicos muestran el éxito de la técnica de RMN en Costa Rica durante los últimos 40 años. No cabe duda de que la investigación costarricense utilizando RMN se ha centrado en la identificación y elucidación estructural de moléculas orgánicas, especialmente aquellas procedentes de productos naturales; estudios mayoritariamente desarrollados por investigadores adscritos al CIPRONA. Estos resultados se deben no solo a la adquisición de los equipos de campo alto instalados en la UCR, sino al capital humano nacional que se ha capacitado en dicha técnica y que ha permitido los avances descritos.
Esta revisión bibliográfica no incluye tesis y proyectos de graduación, pues haría inmanejable las citas bibliográficas debido a la enorme cantidad que se han realizado en más de 40 años, cuando se instaló el primer RMN, y que han utilizado la técnica para sus investigaciones. No obstante, el omitir esta información no impide valorar el rol que ha jugado la RMN en el desarrollo de los profesionales en ciencia y tecnología de este país.
El artículo más antiguo encontrado en las bases de datos, y que utiliza el equipo de RMN instalado en el país, es de 1979. Esto muestra que desde un inicio la técnica fue utilizada en investigaciones locales, aunque es probable que existan otros estudios y publicaciones anteriores, particularmente tesis de grado y proyectos de graduación no registrados en las bases de datos consultadas.
También es importante recalcar que, en los últimos años, la investigación en RMN se ha diversificado, permitiendo que otras áreas del conocimiento la utilicen como herramienta en sus investigaciones. Particularmente, estudios relacionados con biología molecular, sistemas macromoleculares o ingeniería de materiales han empezado a utilizar la técnica. Esto es un paso importante para la democratización de la RMN en Costa Rica, pues ha dejado de ser un bien químico para convertirse en uno multidisciplinario.
La mayoría de los estudios realizados en el país han hecho uso de secuencias de pulsos tradicionales, sobre todo experimentos unidimensionales de 1H y 13C, ROESY (Rotating Frame Overhauser Enhancement Espectroscopy), DEPT, así como aquellos en dos dimensiones tales como COSY, NOESY, HSQC (Heteronuclear Single Quantum Coherence) y HMBC (Heteronuclear Multiple Bond Correlation). La figura 10 muestra la gráfica que relaciona la cantidad de publicaciones en RMN, ya sea realizadas en Costa Rica o que involucren la asesoría de investigadores nacionales en el área, por año. En la figura se incluyen líneas punteadas verticales que marcan los años en que se instalaron los distintos magnetos en Costa Rica.
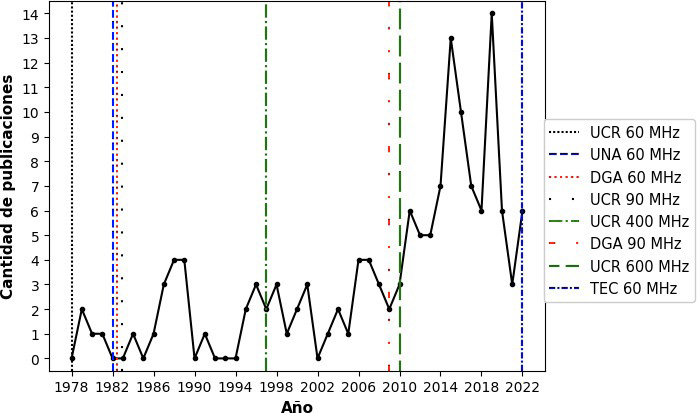
Figura 10. Gráfica de la cantidad estudios científicos realizados en Costa Rica, o por costarricenses, relacionados con la RMN, en función del año en que fueron publicados.
Es claro que el volumen de publicaciones en RMN ha aumentado desde la instalación del primer equipo en la UCR, se mantuvo relativamente constante en la década de los 90’s y creció significativamente en los últimos quince años. Este crecimiento concuerda con el acceso a los equipos de campo alto de 400 MHz y 600 MHz, con su respectiva mejora en la resolución y acceso a nuevos experimentos.
Hasta el momento se ha mencionado el uso de la RMN en investigación, pero no puede dejarse de lado su trascendental papel en la academia. Desde la adquisición del primer equipo de RMN en la UCR, la técnica se ha estudiado y aplicado en cursos de química orgánica y sus laboratorios de las universidades públicas del país, además de en cursos de posgrado. Incluso, se ha escrito un manual de prácticas para el análisis espectral, ampliamente utilizado por estudiantes en universidades públicas y privadas del país [246].
Por otro lado, se han llevado a cabo capacitaciones y talleres en fenómenos de relajación, secuencias de pulsos, sondas criogénicas y aplicaciones varias de la RMN, tanto para docentes como para estudiantes. En los últimos diez años se han ofertado cursos interuniversitarios para el estudio de la RMN en líquidos y sólidos [247]. De hecho, aunque el país no cuenta actualmente con una sonda de sólidos, se han empezado a realizar cursos de capacitación en esta temática, y no solo para estudiantes de las ciencias químicas, sino también para ingenieros y ciencias médicas.
C. Futuro y perspectiva de la RMN en Costa Rica
La inversión en infraestructura, capacitación y desarrollo en RMN puede ayudar a mejorar los índices costarricenses en investigación y desarrollo (I+D), los cuales están muy por debajo de la media de los países de la Organización para la Cooperación y el Desarrollo Económicos (OCDE) [248, 249]. Con la adquisición del equipo de 600 MHz, Costa Rica dio un paso significativo en el desarrollo científico y tecnológico pues puso dicho equipo a disposición de la comunidad científica nacional. Gracias a él, la cantidad de publicaciones y la calidad de las investigaciones aumentó dramáticamente (ver figura 10). No cabe duda de que el país necesitaba de un equipo de campo alto. No obstante, la potencialidad de la técnica de RMN, con los equipos disponibles, aún no ha alcanzado su punto más alto en el país.
La RMN en Costa Rica está pasando por un proceso de renovación y reestructuración, en el que está dejando de ser una técnica utilizada para la identificación y caracterización estructural, para convertirse en un área de investigación, propiamente dicha. Las primeras señales de este proceso se han dado en el terreno pedagógico, preparando a los estudiantes y profesores en los fundamentos teóricos de áreas poco desarrolladas hasta la fecha en el país, y de suma utilidad, como la RMN en estado sólido o los fenómenos de hiperpolarización para la mejora en la intensidad de las señales. La apertura de cursos interuniversitarios ha permitido que estudiantes de diversas áreas del conocimiento estén adquiriendo las destrezas necesarias sobre el estado del arte de la RMN, y sus usos potenciales, no sólo para la química sino para la ciencia y la tecnología en general [247]. Por otro lado, se han venido desarrollando pasantías de estudiantes costarricenses en universidades de prestigio, y con amplia experiencia en RMN, donde han podido utilizar la tecnología vigente en sus investigaciones particulares [228, 229]. Algunos centros de investigación han organizado cursos, talleres y seminarios con expertos internacionales en temas referentes a la RMN en líquidos y sólidos, aprendiendo sobre modificaciones en secuencias de pulsos o el uso de software especializado. Ahora bien, ¿cuáles son las siguientes etapas en este proceso?
i.Desarrollo experimental de la RMN en estado sólido: La adquisición de una sonda de RMN para medición de muestras en estado sólido o semi-sólido es una cuestión de tiempo. El desarrollo en la ingeniería de materiales o los estudios de proteínas y sistemas macromoleculares, campos en los que la mayoría de las muestras en estudio están en estado sólido, hacen necesario la actualización de los equipos disponibles en el país. La realización de experimentos de RMN en estado sólido, mediante MAS y MAS de alta resolución (HR-MAS), permitirá realizar estudios de configuración molecular y electrónica en áreas como el desarrollo de materiales porosos, diseño de drogas, química macromolecular, dinámica de espines o control de calidad en alimentos. Las áreas de aplicación de la RMN en sólidos son muy extensas en el país, por lo que el desarrollo de la técnica será de utilidad no sólo para la academia sino también para la industria costarricense.
ii.Aplicación y desarrollo de nuevas secuencias de pulsos: Los procesos de capacitación, a través de cursos, seminarios y talleres, ha permitido acercar la técnica de RMN a sectores académicos que pueden brindar una perspectiva no vista antes en el país. Por ejemplo, el poder contar con ingenieros físicos, ingenieros de materiales o ingenieros electrónicos, en el estudio de los fundamentos y aplicaciones de la técnica puede permitir el desarrollo de nuevas secuencias de pulsos, tanto en estado líquido como sólido, algo que no se ha realizado directamente en el país. El proceso de innovación que estos desarrollos conllevan puede impulsar a la ciencia de Costa Rica a ámbitos nunca vistos, gracias a un desarrollo multidisciplinar de la RMN.
iii.Democratización de la técnica: Hasta la fecha, todos los equipos de RMN con que ha contado el país han sido accesibles únicamente a los técnicos y a ciertos profesores, lo que ha llevado a un distanciamiento entre los equipos de RMN y sus posibles usuarios, haciendo ver la técnica como lejana y difícil. Con la adquisición de equipos de RMN de escritorio con magneto permanente [103], la técnica se vuelve más accesible a los estudiantes y público en general, pues sus costos de mantenimiento, manejo y facilidad de uso, los hacen sumamente atractivos, a pesar de la pérdida de resolución inherente.
iv.Organización de eventos académicos: Si se quiere avanzar en ciencia es necesario interactuar y crear redes de contacto con expertos internacionales. Poder interactuar con especialistas permite desarrollar nuevas destrezas, y esto no es ajeno a la RMN. Una de las mejores formas de interacción con expertos y especialistas es a partir de la organización de congresos, talleres o capacitaciones. Escuelas de verano en RMN, como las de Leipzig o México, han permitido que estudiantes costarricenses se capaciten en aspectos como fenómenos de relajación, RMN de sólidos o fenómenos de hiperpolarización [250–252]. La organización de eventos científicos relacionados con RMN en el país puede traer grandes ventajas al desarrollo de la técnica y permitir colaboraciones que catalicen este avance.
v.Diseño, construcción y desarrollo local: El país cuenta con capital humano altamente capacitado para el diseño de equipo de RMN, particularmente de campo bajo (1,8 T) y de campo cero y ultra bajo (en el orden de los microteslas), ya que requieren de magnetos permanentes y de dispositivos superconductores de interferencia cuántica (SQUID), fácilmente accesibles. Este desarrollo tecnológico permitiría una mejora en los índices de innovación del país, así como los de I+D, y ayudaría a utilizar los recursos en equipo 100% costarricense.
vi.Adquisición de nuevos equipos de campo alto: La mejor forma de aumentar la resolución de la RMN es aumentando el campo magnético y esto se consigue con magnetos superconductores cada vez más potentes. Actualmente, el equipo de 600 MHz del CIPRONA es el más potente en el país, pero si se desea mejorar en los estudios y avances de RMN es necesario la adquisición de nuevos equipos con campos magnéticos más altos. La presente situación financiera del país, junto con los altos costos de los sistemas criogénicos, hace muy difícil que pueda adquirirse un nuevo equipo, pero esto no quiere decir que el mismo no sea una necesidad y un paso más para el desarrollo de la ciencia y la tecnología costarricense. Es una gran inversión, pero se ha demostrado que la RMN trae consigo investigaciones de alto nivel, publicaciones de calidad y un impacto mayúsculo al desarrollo del país.
Queda mucho por hacer, pero el proceso que inició hace ya varios años es constante y va dando pasos seguros y confiables. Son muchos los avances que el país ha realizado desde la adquisición del primer equipo allá por la década de los 70’s, pero son aún más los cambios por venir, si el país y la ciencia, a través de sus universidades y centros de investigación, dedican más de sus recursos humanos y materiales al desarrollo de la RMN.
Agradecimientos
Los autores agradecen al Centro de Investigación y Servicios Químicos y Microbiológicos (CEQIATEC) por el apoyo financiero para la realización de esta investigación, así como a todas aquellas personas que participaron en las entrevistas y cuya información fue fundamental para la escritura del presente documento.
Referencias
[1] N. Waksman Minsky y A. Saucedo Yáñez, “Breve historia de la Resonancia Magnética Nuclear: desde el descubrimiento hasta la aplicación en imagenología”, Educación Química, vol. 30, n.º 2, p. 129, abril de 2019. https://doi.org/10.22201/fq.18708404e
.2019.2.68418
[2] M. H. Levitt, Spin Dynamics: Basics of Nuclear Magnetic Resonance. John Wiley and Sons Inc, 2008.
[3] “National Nuclear Data Center”. Brookhaven National Laboratory. https://www.nndc.bnl.gov/nudat3/. (accedido el 12 de mayo de 2023).
[4] D. L. Pavia, Introduction to Spectroscopy, 4a ed. Brooks Cole, 2008.
[5] M.K. Singh y A. Singh, Nuclear Magnetic Resonance Spectroscopy, Characterization of Polymers and Fibers, Chapter 14, pp. 321-339, 2022.
[6] V. G. Kiselev, “Larmor frequency in heterogeneous media”, Journal of Magnetic Resonance, vol. 299, pp. 168–175, febrero de 2019. https://doi.org/10.1016/j.jmr
.2018.12.008
[7] M. G. Morris, “NMR Data Processing”, Encyclopedia of Spectroscopy and Spectrometry, 3a ed., pp. 125-133, 2017. https://doi.org/10.1016/B978-0-12-409547-2.05103-9
[8] T. Yamazaki y A. Takatsu, “Quantitative NMR spectroscopy for accurate purity determination of amino acids, and uncertainty evaluation for different signals”, Accreditation and Quality Assurance, vol. 19, n.º 4, pp. 275–282, julio de 2014. https://doi.org/10.1007/s00769-014-1067-2
[9] O. Mertins, M. Sebben, P. Henrique Schneider, A. R. Pohlmann y N. P. d. Silveira, “Caracterização da pureza de fosfatidilcolina da soja através de RMN de ¹H e de 31P”, Química Nova, vol. 31, n.º 7, pp. 1856–1859, 2008. https://doi.org/10.1590/s0100-40422008000700043
[10] N. Uchiyama et al., “Purity Determination of Cyclophosphamide Hydrate by Quantitative 31P-NMR and Method Validation”, Chemical and Pharmaceutical Bulletin, vol. 69, n.º 7, pp. 630–638, julio de 2021. https://doi.org/10.1248/cpb.c21-00109
[11] N. Uchiyama et al., “Absolute Purity Determination of a Hygroscopic Substance, Indocyanine Green, Using Quantitative NMR (qNMR)”, Chemical and Pharmaceutical Bulletin, vol. 69, n.º 1, pp. 118–123, enero de 2021. https://doi.org/10.1248/cpb.c
20-00728
[12] T. Schoenberger, “Determination of standard sample purity using the high-precision 1H-NMR process”, Analytical and Bioanalytical Chemistry, vol. 403, n.º 1, pp. 247–254, febrero de 2012. https://doi.org/10. 1007/s00216-012-5777-1
[13] P. A. Hays, “Proton nuclear magnetic resonance spectroscopy (NMR) methods for determining the purity of reference drug standards and illicit forensic drug seizures”, Journal of Forensic Sciences, vol. 50, n.º 6, pp. 1–19, 2005. https://doi.org/10.152
0/jfs2005124
[14] M. Cushman, G. I. Georg, U. Holzgrabe y S. Wang, “Absolute Quantitative 1H NMR Spectroscopy for Compound Purity Determination”, Journal of Medicinal Chemistry, vol. 57, n.º 22, p. 9219, noviembre de 2014. https://doi.org/10.1021/jm501683w
[15] D. Parker, “NMR determination of enantiomeric purity”, Chemical Reviews, vol. 91, n.º 7, pp. 1441–1457, noviembre de 1991. https://doi.org/10.1021/cr00007a009
[16] C. Simmler, J. G. Napolitano, J. B. McAlpine, S.-N. Chen y G. F. Pauli, “Universal quantitative NMR analysis of complex natural samples”, Current Opinion in Biotechnology, vol. 25, pp. 51–59, febrero de 2014. https://doi.org/10.1016/j.cop
bio.2013.08.004
[17] D. P. Nicolella, Q. Ni y K. S. Chan, “Non-destructive characterization of microdamage in cortical bone using low field pulsed NMR”, Journal of the Mechanical Behavior of Biomedical Materials, vol. 4, n.º 3, pp. 383–391, abril de 2011. https://doi.org/1
0.1016/j.jmbbm.2010.11.007
[18] A. Adams, “Non-destructive analysis of polymers and polymer-based materials by compact NMR”, Magnetic Resonance Imaging, vol. 56, pp. 119–125, febrero de 2019. https://doi.org/10.1016/j.mri.2018.09.015
[19] M. V. Silva Elipe et al., “Application and Methodology of the Non-destructive 19F Time-domain NMR Technique to Measure the Content in Fluorine-containing Drug Products”, Journal of Visualized Experiments, n.º 126, agosto de 2017. https://doi.or
g/10.3791/55850
[20] Y. Nakashima, “Non-Destructive Quantification of Lipid and Water in Fresh Tuna Meat by a Single-Sided Nuclear Magnetic Resonance Scanner”, Journal of Aquatic Food Product Technology, vol. 28, n.º 2, pp. 241–252, enero de 2019. https://doi.or
g/10.1080/10498850.2019.1569742
[21] B. Blümich, Y. Teymouri y R. Clark, “NMR on the Road: Non-destructive Characterization of the Crumb-Rubber Fraction in Asphalt”, Applied Magnetic Resonance, vol. 50, n.º 1-3, pp. 497–509, noviembre de 2018. https://doi.org/10.10
07/s00723-018-1097-8
[22] F. Braun y J. Orlowsky, “Non-destructive detection of the efficiency of long-term weathered hydrophobic natural stones using single-sided NMR”, Journal of Cultural Heritage, vol. 41, pp. 51–60, enero de 2020. https://doi.org/10.1016/j.culher.201
9.07.005
[23] A. Melado-Herreros, M. E. Fernández-Valle y P. Barreiro, “Non-Destructive Global and Localized 2D T1/T2 NMR Relaxometry to Resolve Microstructure in Apples Affected by Watercore”, Food and Bioprocess Technology, vol. 8, n.º 1, pp. 88–99, agosto de 2014. https://doi.org/10.1007/s11947-014-1389-4
[24] S. Keine, R. Schulte Holthausen y M. Raupach, “Single-sided NMR as a non-destructive method for quality evaluation of hydrophobic treatments on natural stones”, Journal of Cultural Heritage, vol. 36, pp. 128–134, marzo de 2019. https://doi.org/10.1016/j.culher.2018.07.012
[25] G. A. Boyle, H. G. Kruger, G. E. M. Maguire y A. Singh, “NMR elucidation of some pentacycloundecane derived ligands”, Structural Chemistry, vol. 18, n.º 5, pp. 633–639, junio de 2007. https://doi.org/10.1007/s11224-007-9190-x
[26] O. K. Onajole, P. Govender, T. Govender, G. E. M. Maguire y H. G. Kruger, “NMR elucidation of novel SQ109 derivatives”, Structural Chemistry, vol. 21, n.º 6, pp. 1203–1209, octubre de 2010. https://doi.org/10. 1007/s11224-010-9661-3
[27] M. S. Altaib et al., “Synthesis and NMR elucidation of novel pentacycloundecane-based peptides”, Magnetic Resonance in Chemistry, pp. 435-442, 2010. https://doi.org/10.1002/mrc.2598
[28] E. Kupce y T. D. W. Claridge, “NOAH: NMR Supersequences for Small Molecule Analysis and Structure Elucidation”, Angewandte Chemie International Edition, vol. 56, n.º 39, pp. 11779–11783, agosto de 2017. https://doi.org/10.1002/anie.20
1705506
[29] M. T. Kelani et al., “Trends in NMR Structural Elucidation Of Polycyclic Cages, Namely: Adamantane, Pentacycloundecane and Trishomocubane”, South African Journal of Chemistry, vol. 75, 2021. https://doi.org/10.17159/0379-4350/2021/v75a
14
[30] A. K. Korir y C. K. Larive, “On-line NMR detection of microgram quantities of heparin-derived oligosaccharides and their structure elucidation by microcoil NMR”, Analytical and Bioanalytical Chemistry, vol. 388, n.º 8, pp. 1707–1716, julio de 2007. https://doi.org/10.1007/s00216-007-1400-2
[31] M. Shaikh, K. Petzold, H. G. Kruger y K. du Toit, “Synthesis and NMR elucidation of homoisoflavanone analogues”, Structural Chemistry, vol. 22, n.º 1, pp. 161–166, diciembre de 2010. https://doi.org/10.1007/s11224-010-9703-x
[32] A. T. Á. Pimenta, R. Braz-Filho, P. G. Delprete, E. B. de Souza, E. R. Silveira y M. A. S. Lima, “Structure elucidation and NMR assignments of two unusual monoterpene indole alkaloids from Psychotria stachyoides”, Magnetic Resonance in Chemistry, vol. 48, n.º 9, pp. 734–737, julio de 2010. https://doi.org/10.1002/mrc.2656
[33] Z. Huang, R. Yang, X. Yin, Z. She y Y. Lin, “Structure elucidation and NMR assignments for two xanthone derivatives from a mangrove endophytic fungus (No. ZH19)”, Magnetic Resonance in Chemistry, vol. 48, n.º 1, pp. 80–82, noviembre de 2009. https://doi.org/10.1002/mrc.2539
[34] A. P. Tikunov, C. B. Johnson, H. Lee, M. K. Stoskopf y J. M. Macdonald, “Metabolomic Investigations of American Oysters Using 1H-NMR Spectroscopy”, Marine Drugs, vol. 8, n.º 10, pp. 2578–2596, octubre de 2010. https://doi.org/10.3390/md8102578
[35] A. Metere, C. E. Graves, M. Chirico, M. J. Caramujo, M. E. Pisanu y E. Iorio, “Metabolomic Reprogramming Detected by 1H-NMR Spectroscopy in Human Thyroid Cancer Tissues”, Biology, vol. 9, n.º 6, p. 112, mayo de 2020. https://do
i.org/10.3390/biology9060112
[36] H.-K. Choi, J.-H. Yoon, Y.-S. Kim y D. Y. Kwon, “Metabolomic profiling of Cheonggukjang during fermentation by 1H NMR spectrometry and principal components analysis”, Process Biochemistry, vol. 42, n.º 2, pp. 263–266, febrero de 2007. https://doi.org/10.1016/j.procbio.2006.07.014
[37] I. J. Lee, K. Hom, G. Bai y M. Shapiro, “NMR Metabolomic Analysis of Caco-2 Cell Differentiation”, Journal of Proteome Research, vol. 8, n.º 8, pp. 4104–4108, agosto de 2009. https://doi.org/10.1021/pr8010759
[38] D. V. Luong, N. Q. Tam, D. T. T. Xuan y N. T. Tai, “NMR based metabolomic approach for evaluation of Vietnamese honey”, Vietnam Journal of Chemistry, vol. 57, n.º 6, pp. 712–716, diciembre de 2019. https://doi.org/10.1002/vjch.2019000101
[39] H.-K. Choi y J.-H. Yoon, “Metabolomic profiling of Vitis vinifera cell suspension culture elicited with silver nitrate by 1H NMR spectrometry and principal components analysis”, Process Biochemistry, vol. 42, n.º 2, pp. 271–274, febrero de 2007. https://doi.org/10.1016/j.procbio.2006.07.007
[40] L. Sirelli, R. M. K. Prado, M. I. B. Tavares, R. C. R. Nunes y M. L. Dias, “Molecular Dynamics of Poly(Ethylene Terephthalate)/Muscovite Mica Composite by Low-Field NMR”, International Journal of Polymer Analysis and Characterization, vol. 13, n.º 3, pp. 180–189, mayo de 2008. https://doi.org/10.1080/10236660802070678
[41] U. Sternberg y R. Witter, “Molecular dynamics simulations on PGLa using NMR orientational constraints”, Journal of Biomolecular NMR, vol. 63, n.º 3, pp. 265–274, septiembre de 2015 https://doi.org/10.1007/s10858-015-9983-y
[42] H. Omichi, T. Ueda y T. Eguchi, “Molecular motion of alcohols adsorbed in ACF hydrophobic nanoslits as studied by solid-state NMR”, Adsorption, vol. 21, n.º 4, pp. 273–282, abril de 2015. https://doi.org/10.1007/s10450-015-9669-5
[43] Y. Fu, H. Guan, J. Yin y X. Kong, “Probing molecular motions in metal-organic frameworks with solid-state NMR”, Coordination Chemistry Reviews, vol. 427, p. 213563, enero de 2021. https://doi.org/10.1016/j.ccr.2020. 213563
[44] H. Omichi, T. Ueda, Y. Chen, K. Miyakubo y T. Eguchi, “Specific Molecular Motion of Adamantane Induced by Hydrophobic Nanoslits in ACF as Studied Using Solid-State 1H, 2H, and 13C NMR”, Molecular Crystals and Liquid Crystals, vol. 490, n.º 1, pp. 91–105, septiembre de 2008. https://doi.org/10.1080/15421400802305772
[45] V. Domenici, T. Apih y C. A. Veracini, “Molecular motions of banana-shaped liquid crystals studied by NMR spectroscopy”, Thin Solid Films, vol. 517, n.º 4, pp. 1402–1406, diciembre de 2008. https://doi.org/10.1016/j.tsf. 2008.09.035
[46] G. P. Lisi y J. Patrick Loria, “Using NMR spectroscopy to elucidate the role of molecular motions in enzyme function”, Progress in Nuclear Magnetic Resonance Spectroscopy, vol. 92-93, pp. 1–17, febrero de 2016. https://doi.org/10.1016/j.pnm
rs.2015.11.001
[47] O. Fricová, M. Hutníková, M. Kovalaková y A. Baran, “Influence of aging on molecular motion in PBAT-thermoplastic starch blends studied using solid-state NMR”, International Journal of Polymer Analysis and Characterization, vol. 25, n.º 4, pp. 275–282, mayo de 2020. https://doi.org/10.1080/1023666x.2020.1783495
[48] C. G. Kalodimos, “NMR reveals novel mechanisms of protein activity regulation”, Protein Science, vol. 20, n.º 5, pp. 773–782, abril de 2011. https://doi.org/10.1002/p
ro.614
[49] B. Baminger, M. L. Ludwiczek, G. Kontaxis, S. Knapp y R. Konrat, “Protein–protein interaction site mapping using NMR-detected mutational scanning”, Journal of Biomolecular NMR, vol. 38, n.º 2, pp. 133–137, abril de 2007. https://doi.org/10.100
7/s10858-007-9154-x
[50] A. Loquet, C. Gardiennet y A. Böckmann, “Protein 3D structure determination by high-resolution solid-state NMR”, Comptes Rendus Chimie, vol. 13, n.º 4, pp. 423–430, abril de 2010. https://doi.org/10.1016/j.crci.2010.03.007
[51] M. Dreydoppel, J. Balbach y U. Weininger, “Monitoring protein unfolding transitions by NMR-spectroscopy”, Journal of Biomolecular NMR, vol. 76, n.º 1-2, pp. 3–15, enero de 2022. https://doi.org/10.1007/s10858-021-00389-3
[52] C. Li, C. Tang y M. Liu, “Protein dynamics elucidated by NMR technique”, Protein and Cell, vol. 4, n.º 10, pp. 726–730, septiembre de 2013. https://doi.org/10.1007/s1323
8-013-3912-1
[53] D. R. Jensen et al., “Rapid, robotic, small-scale protein production for NMR screening and structure determination”, Protein Science, vol. 19, n.º 3, pp. 570–578, enero de 2010. https://doi.org/10.1002/pro.335
[54] M. J. Duer, Introduction to Solid-State NMR Spectroscopy. Wiley-Blackwell, 2005.
[55] B. Reif, S. E. Ashbrook, L. Emsley y M. Hong, Solid-State NMR Spectroscopy. Nature Reviews Methods Primers, 2021.
[56] F. W. Sears y R. A. Freedman, Física Universitaria con Fisica Moderna Volumen 2. Naucalpan de Juarez, Estado de Mexico: Pearson Educacion, 2009.
[57] C. Eccles, “Low Field NMR Methods and Applications”, Encyclopedia of Spectroscopy and Spectrometry, pp. 611-626, octubre de 2016. https://doi.org/10.1016/B978-0-12-409547-2.05099-X
[58] E. O. Fridjonsson, S. J. Vogt, J. S. Vrouwenvelder y M. L. Johns, “Early non-destructive biofouling detection in spiral wound RO membranes using a mobile earth’s field NMR”, Journal of Membrane Science, vol. 489, pp. 227–236, setiembre de 2015. https://doi.org/10.1016/j.memsci.2015.03.088
[59] M. S. Conradi, S. A. Altobelli, N. J. Sowko, S. H. Conradi y E. Fukushima, “Earth’s field NMR detection of oil under arctic ice–water suppression”, Journal of Magnetic Resonance, vol. 288, pp. 95–99, marzo de 2018. https://doi.org/10.1016/j.jmr.20
18.02.004
[60] M. E. Halse, P. T. Callaghan, B. C. Feland y R. E. Wasylishen, “Quantitative analysis of Earth’s field NMR spectra of strongly-coupled heteronuclear systems”, Journal of Magnetic Resonance, vol. 200, n.º 1, pp. 88–94, septiembre de 2009. https://doi.org
/10.1016/j.jmr.2009.06.012
[61] E. O. Fridjonsson, L. S. Flux y M. L. Johns, “Determination of mean droplet sizes of water-in-oil emulsions using an Earth’s field NMR instrument”, Journal of Magnetic Resonance, vol. 221, pp. 97–102, agosto de 2012. https://doi.org/10.1016/j.jmr.201
2.05.012
[62] I. F. Céspedes-Camacho y J. Matysik, “Solid-state NMR and hyperpolarization methods for the Research, Development, and Innovation in Costa Rican science”, Biophysical Rev., marzo de 2022. https://doi.org/10.1007/s12551-022-00946-6
[63] I. I. Rabi, J. M. B. Kellogg y J. R. Zacharias, “The Magnetic Moment of the Proton”, Physical Review, vol. 46, n.º 3, pp. 157–163, agosto de 1934. https://doi.org/10.110
3/physrev.46.157
[64] I. I. Rabi, J. R. Zacharias, S. Millman y P. Kusch, “A New Method of Measuring Nuclear Magnetic Moment”, Physical Review, vol. 53, n.º 4, p. 318, febrero de 1938. https://doi.org/10.1103/physrev.53.318
[65] C. J. Giunta y V. V. Mainz, “Discovery of Nuclear Magnetic Resonance: Rabi, Purcell, and Bloch”, ACS Symposium Series, vol. 1349, n.° 1, pp. 3-20, abril de 2020. https://doi.org/10.1021/bk-2020-1349.ch001
[66] R. Frisch y O. Stern, “Über die magnetische Ablenkung von Wasserstoffmolekülen und das magnetische Moment des Protons. I”, Zeitschrift für Physik, vol. 85, n.º 1-2, pp. 4–16, enero de 1933. https://doi.org/10.1007/bf01330773
[67] E. M. Purcell, H. C. Torrey y R. V. Pound, “Resonance Absorption by Nuclear Magnetic Moments in a Solid”, Physical Review, vol. 69, n.º 1-2, pp. 37–38, enero de 1946. https://doi.org/10.1103/physrev.69.37
[68] F. Bloch, “Nuclear Induction”, Physical Review, vol. 70, n.º 7-8, pp. 460–474, octubre de 1946. https://doi.org/10.1103/physrev.70.460
[69] J. T. Arnold, S. S. Dharmatti y M. E. Packard, “Chemical Effects on Nuclear Induction Signals from Organic Compounds”, The Journal of Chemical Physics, vol. 19, n.º 4, p. 507, abril de 1951. https://doi.org/10.1063/1.1748264
[70] G. E. Pake, “Nuclear Resonance Absorption in Hydrated Crystals: Fine Structure of the Proton Line”, The Journal of Chemical Physics, vol.16, n.º 4, pp. 327–336, abril de 1948. https://doi.org/10.1063/1.1746878
[71] E. R. Andrew, A. Bradbury y R. G. Eades, “Nuclear Magnetic Resonance Spectra from a Crystal rotated at High Speed”, Nature, vol. 182, n.º 4650, p. 1659, diciembre de 1958. https://doi.org/10.1038/1821659a0
[72] P. Chen et al., “Magic angle spinning spheres”, Science Advances, vol. 4, n.º 9, septiembre de 2018. https://doi.org/10.1126/sciadv.aau1540
[73] R. R. Ernst y W. A. Anderson, “Application of Fourier Transform Spectroscopy to Magnetic Resonance”, Review of Scientific Instruments, vol. 37, n.º 1, pp. 93–102, enero de 1966. https://doi.org/10.1063/1.1719961
[74] R. Gantes, “Técnicas de reconstrucción de imagen en Resonancia Magnética”, Tesis de maestría, Universidad Complutense de Madrid, 2009. Accedido el 5 de enero de 2023. [En línea]. Disponible: http://nuclear.fis.ucm.es/research/thesis/TM-Rosa-Gantes.pdf
[75] W. P. Aue, E. Bartholdi y R. R. Ernst, “Two-dimensional spectroscopy. Application to nuclear magnetic resonance”, The Journal of Chemical Physics, vol. 64, n.º 5, pp. 2229–2246, marzo de 1976. https://doi.org/10.1063/1.432450
[76] G. Wagner, W. Braun, T. F. Havel, T. Schaumann, N. Go y K. Wüthrich, “Protein structures in solution by nuclear magnetic resonance and distance geometry”, Journal of Molecular Biology, vol. 196, n.º 3, pp. 611–639, agosto de 1987. https://doi.org/10.1016/0022-2836(87)90037-4
[77] C. Bettenhausen, “Bruker installs world’s first 1.2 GHz”, Chemical & Engineering News, 15 de mayo de 2020. Accedido el 13 de mayo de 2023, [En línea]. Disponible: https://cen.acs.org/business/instrumentation/Bruker-installs-12-GHz-NMR/98/i19
[78] J. Ecker, “Eight tons of hope: world’s strongest persistent magnet for NMR at ETH”, Departement Chemie und Angewandte Biowissenschaften, ETH Zürich, junio de 2020. Accedido el 13 de mayo de 2023. [En línea]. Disponible: https://chab.ethz.ch/en/news-and-events/d-chab-news/2020/06/8-tons-of-hope-worlds-strongest-nmr-magnet-at-eth.html
[79] B. Blümich, “Low-field and benchtop NMR”, J. Magnetic Reson., vol. 306, pp. 27–35, septiembre de 2019. https://doi.org/10.1016/j.jmr.2019.07.030
[80] J, Giberson, J. Scicluna, N. Legge y J. Longstraffe, “Chapter Three - Developments in benchtop NMR spectroscopy 2015–2020”, Annual Reports on NMR Spectroscopy., vol. 102, pp. 153–246, 2021. https://doi.org/10.1016/bs.arnmr.2020.10.006
[81] T. Castaing-Cordier, D. Bouillaud, J. Farjon y P. Giraudeau, “Chapter Four - Recent advances in benchtop NMR spectroscopy and its applications”, Annual Reports on NMR Spectroscopy., vol. 103, pp. 191–258, 2021. https://doi.org/10.1016/bs.arn
mr.2021.02.003
[82] M. Grootveld et al., “Progress in low-field benchtop NMR spectroscopy in chemical and biochemical analysis”, Analytica Chimica Acta, vol. 1067, pp. 11–30, agosto de 2019. https://doi.org/10.1016/j.aca.2019.02.026
[83] J. F. Araneda et al., “Incorporating Benchtop NMR Spectrometers in the Undergraduate Lab: Understanding Resolution and Circumventing Second-Order Effects”, J. Chem. Educ., vol. 98, n.º 4, pp. 1227–1232, febrero de 2021. https://doi.org/10.1021/acs.jchemed.0c01182
[84] S. D. Riegel y G. M. Leskowitz, “Benchtop NMR spectrometers in academic teaching”, TrAC Trends Analytical Chemistry, vol. 83, pp. 27–38, octubre de 2016. https://doi.org/10.1016/j.trac.2016.01.001
[85] M. Hunter, “Chapter 4 - Earth’s Field Spectroscopy”, Annual Reports on NMR Spectroscopy, vol. 76, pp. 139-164, 2012. https://doi.org/10.1016/B978-0-12-397019-0.00004-2
[86] L. T. Kuhn, Ed., Hyperpolarization Methods in NMR Spectroscopy. Berlin, Heidelberg: Springer Berlin Heidelberg, 2013. https://doi.org/10.1007/978-3-642-39728-8
[87] P. Pham, R. Mandal, C. Qi y C. Hilty, “Interfacing Liquid State Hyperpolarization Methods with NMR Instrumentation”, J. Magnetic Reson. Open, vol. 10-11, p. 100052, junio de 2022. https://doi.org/10.1016/j.jmro.2022.100052
[88] M.A. Calvo-Pineda, “Entrevista sobre la historia y el desarrollo de la RMN en la UNA”, Comunicación personal (13 de junio, 2023).
[89] J. Vargas-León, “Entrevista sobre equipos de RMN de Perkin-Elmer en Costa Rica”, Comunicación personal (13 de junio, 2023).
[90] G. Tamayo-Castillo, “Entrevista sobre la historia de la RMN en la UCR y el CIPRONA”, Comunicación personal (26 de setiembre, 2022).
[91] University of Nairobi, “Achievements and Milestones”, University Of Nairobi| Department Of Chemistry. https://chemistry.uonbi.ac.ke/basic-page/achievements-and-milestones (accedido el 21 de junio de 2023).
[92] M. Condren. “Nuclear Magnetic Resonance Instruments”. Interdisciplinary Education Group. https://chem.beloit.edu/edetc/background/NMR/NMRinstru.h
tml (accedido el 21 de junio de 2023).
[93] E. Lanzoni-Vindas, “Entrevista sobre historia y uso de RMN en Laboratorio de Aduanas de Costa Rica”, Comunicación personal (17 de julio, 2023).
[94] A. Villalobos-Chaves, “Entrevista sobre el uso y experiencia con los equipos de RMN del Laboratorio de Aduanas de Costa Rica”, Comunicación personal (17 de julio, 2023).
[95] S.M. Diab y G.A. Moehring, “WWW-based remote FT-NMR operation: A boost to undergraduated chemistry curriculum and research”, presentado en la 231st ACS Spring National Meeting, Atlanta, Estados Unidos, 2006.
[96] L. Díaz-Sánchez, “Entrevista sobre la experiencia en el manejo de los primeros equipos de RMN en la UCR”, Comunicación personal (21 de junio, 2023).
[97] A. Hernández. “Historia”. CIPRONA, Universidad de Costa Rica (UCR). Octubre, 2018. http://ciprona.ucr.ac.cr/historia/#:~:text=El00%20CIPRONA%20fue%20creado%20a,de%20Qu%C3%83%20mica%20de%20la%20UCR. (Accedido el 5 de enero de 2023).
[98] Instituto Nacional de Biodiversidad (INBio), “Bioprospección: Unidad de espectroscopia de resonancia magnética nuclear”. http://www.inbio.eas.ualber
ta.ca/es/inbio/inb_prosprmn.htm (accedido el 7 de enero de 2023).
[99] “Varian Mercury 400 MHz Nuclear Magnetic Resonance System”. College of Science and Mathematics, Rowan University. https://csm.rowan.edu/departments/chembi
o/instruments/varian-mercury-400mhz-nuclear-magnetic-resonance-system.html (accedido el 7 de enero de 2023).
[100] E. Espinoza-Castellón, “Experiencia sobre el manejo y usos de los RMN del Laboratorio de Aduanas de Costa Rica”, Comunicación personal, (17 de julio, 2023).
[101] Anasazi Instruments. “EFT-90 NMR Spectrometers”. Anasazi Instruments. https://www.aiinmr.com/eft-90/ (accedido el 18 de julio de 2023).
[102] M. Peña y M. Segura, “Nuevo espectrómetro de resonancia magnética”, Universidad de Costa Rica, 4 de noviembre de 2011. Accedido el 7 de enero de 2023, [En línea]. Disponible: https://www.ucr.ac.cr/noticias/2011/11/04/nuevo-espectometro-de-resonancia-magnetica.html
[103] K. Mora-Pérez, “TEC impulsa investigación y conocimiento de la Resonancia Magnética Nuclear”, Hoy en el TEC, 19 de enero de 2023. Accedido el 6 de julio de 2023, [En línea]. Disponible: https://www.tec.ac.cr/hoyeneltec/2023/01/19/tec-impulsa-investigacion-conocimiento-resonancia-magnetica-nuclear
[104] J. A. Cabezas, “Nueva síntesis de la feromona sexual de la polilla del repollo Plutella xylostella”, Ing. Cienc. Quím., vol. 23, n.º 2, 2007.
[105] J. A. Cabezas, “Una nueva ruta para la síntesis de la feromona sexual de la polilla de la papa, Scrobipalpopsis solanivora”, Ing. Cienc. Quím., vol. 18, n.º 2, 1998.
[106] A. C. Fernández-Montalto y G. Valle-Bourrouet, “Síntesis y caracterización de complejos metálicos con el ligando Tris(2- salicilamidoetil)amina”, Ing. Cienc. Quím., vol. 17, n.º 2, 1997.
[107] V. Castro y U. Warning, “Steiractinolides from zexmenia virgulata and constitutents from other compositae from Costa Rica”, Ing. Cienc. Quím., vol. 11, n.º 1, 1987.
[108] C. Hasbun y O. Castro, “Amyris Barbata Lundell: constituyentes mayoritarios de su madera”, Ing. Cienc. Quím., vol. 11, n.º 4, 1987.
[109] A. L. Pérez y J. F. Cicció, “Síntesis de acetales de α-dicetonas aromáticas utilizando una resida intercambiadora catiónica Dowex 50W-X2”, Ing. Cienc. Quím., vol. 13, n.º 2, octubre de 1991.
[110] J. A. Cabezas, J. G. Calzada, V. H. Soto, S. Musmanni y J. F. Cicció, “Síntesis de la feromona sexual de la polilla de la papa, scrobipalpopsis solanivora”, Ing. Cienc. Quím., vol. 12, n.º 3-4, 1988.
[111] J. F. Cicció y R. Procúpez, “Cumarinas de las hojas de myrrhidendron Donnell-Smithii (Apiaceae)”, Ing. Cienc. Quím., vol. 15, n.º 1-2, 1995.
[112] V. Castro, E. Mojica y J. Calzada, “Tres nuevos diterpenos de gyminda costarricensis standl”, Ing. Cienc. Quím., vol. 10, n.º 1-2, 1986.
[113] H. Achenbach, M. Stöcker y M. A. Constenla, “Flavonoid and other constituents of Bauhinia manca”, Phytochemistry, vol. 27, n.º 6, pp. 1835–1841, enero de 1988. https://doi.org/10.1016/0031-9422(88)80455-2
[114] D. Arias y M. A. Constela, “Nota sobre la preparación de un dication cuaternario de azufre divalente”, Quim. Org. UCR, 1979. Accedido el 27 de agosto de 2023. [En línea]. Disponible: https://www.kerwa.ucr.ac.cr/bitstream/handle/10669/89404/N
ota%20sobre%20la%20preparaci%C3%83s%C2%B8n%20de%20un%20dicati%C3%83s%C2%B8n.pdf?sequence=1&isAllowed=y
[115] M. Mundina et al., “Composition and chemical polymorphism of the essential oils from Piper lanceaefolium”, Biochem. Systematics Ecol., vol. 29, n.º 7, pp. 739–748, julio de 2001. https://doi.org/10.1016/s0305-1978(00)00103-4
[116] F. Bohlmann, G. Schmeda-Hirschmann, J. Jakupovic, V. Castro, J. F. Ciccio y G. Calvo, “Further 6,12-cis-Germacranolides and Eudesmanoli- des from Montanoa Species”, J. Natural Products, vol. 47, n.º 4, pp. 663–672, julio de 1984. https://doi.org/
10.1021/np50034a016
[117] J. F. Cicció y J. Calzada, “Haagenolide, the major sesquiterpene lactone of Baltimora recta”, Phytochemistry, vol. 20, n.º 3, p. 517, marzo de 1981. https://doi.org/1
0.1016/s0031-9422(00)84181-3
[118] J. Calzada, J. F. Ciccio y G. Echandi, “Antimicrobial activity of the heliangolide chromolaenide and related sesquiterpene lactones”, Phytochemistry, vol 19, n.º 5, pp. 967-968, 1980. https://doi.org/10.1016/0031-9422(80)85151-X
[119] D. Esquivel-Alvarado, R. Muñoz-Arrieta, E. Alfaro-Viquez, S. Madrigal-Carballo, C. G. Krueger y J. D. Reed, “Composition of Anthocyanins and Proanthocyanidins in Three Tropical Vaccinium Species from Costa Rica”, J. Agricultural Food Chemistry , vol. 68, n.º 10, pp. 2872–2879, junio de 2019. https://doi.org/10.1021/acs.jafc.9b01451
[120] F. A. Venegas et al., “The Bacterial Product Violacein Exerts an Immunostimulatory Effect Via TLR8”, Scientific Reports, vol. 9, n.º 1, septiembre de 2019. https://doi.org/10.1038/s41598-019-50038-x
[121] A. L. Perez, G. Lamoureux y A. Herrera, “Synthesis of Iodinated Naphthoquinones Using Morpholine-Iodine Complex”, Synthetic Communications, vol. 34, n.º 18, pp. 3389–3397, enero de 2004. https://doi.org/10. 1081/scc-200030621
[122] G. Lamoureux, M. Alvarado-Rojas y L. W. Pineda, “Crystal structure of 4-[(adamantan-1-yl)amino]naphthalene-1,2-dione”, Acta Crystallo- graphica Sect. E Crystallographic Commun., vol. 75, n.º 1, pp. 99–102, enero de 2019. https://doi.org/10.1107/s2056989018017917
[123] S. Alvarado, J. F. Ciccio, J. Caldaza, V. Zabel y W. H. Watson, “Thieleanine, a new guaianolide from Decachaeta thieleana”, Phytochemistry, vol. 18, n.º 2, p. 330, enero de 1979. https://doi.org/10.1016/0031-9422(79)80088-6
[124] K. C.-C. Cheng et al., “Actinoramide A Identified as a Potent Antimalarial from Titration-Based Screening of Marine Natural Product Extracts”, Journal of Natural Products, vol. 78, n.º 10, pp. 2411–2422, octubre de 2015. https://doi.or
g/10.1021/acs.jnatprod.5b00489
[125] A. Sidhu et al., “Borrelidin Induces the Unfolded Protein Response in Oral Cancer Cells and Chop-Dependent Apoptosis”, ACS Medicinal Chemistry Letters, vol. 6, n.º 11, pp. 1122–1127, septiembre de 2015. https://doi.org/10.1021/acsmedchem
lett.5b00133
[126] R. M. Schweiggert et al., “Carotenoids, carotenoid esters, and anthocyanins of yellow-, orange-, and red-peeled cashew apples (Anacardium occidentale L.)”, Food Chemistry, vol. 200, pp. 274–282, junio de 2016. https://doi.org/10.1016/j.foo
dchem.2016.01.038
[127] J. Cicció y C. Ballestero, “Constituyentes volátiles de las hojas y espigas de <i>Piper aduncum</i>(Piperaceae) de Costa Rica”, Revista De Biología Tropical, vol. 45, n.º 2, pp. 783–790, 2015. Accedido el 10 de enero de 2023. [En línea]. Disponible: https://revistas.ucr.ac.cr/index. php/rbt/article/view/20868
[128] A. L. Perez, G. Lamoureux y A. Sánchez-Kopper, “Efficient syntheses of streptocarpone and (±)-α-dunnione”, Tetrahedron Letters, vol. 48, n.º 21, pp. 3735–3738, mayo de 2007. https://doi.org/10.1016/j.tetlet.2007.03.090
[129] M. Ledezma-Gairaud, L. W. Pineda, G. Aromí y E. C. Sañudo, “Microwave assisted synthesis: A Mn/Ni reaction system affording Mn5Ni4, Mn2Ni2 and Mn7 complexes”, Polyhedron, vol. 64, pp. 45–51, noviembre de 2013. https://doi.org/10.1016/j.poly.2013.02.018
[130] P. G. Cruz et al., “Novel Lobophorins Inhibit Oral Cancer Cell Growth and Induce Atf4- and Chop-Dependent Cell Death in Murine Fibroblasts”, ACS Medicinal Chemistry Letters, vol. 6, n.º 8, pp. 877–881, julio de 2015. https://doi.org/10.1021/acsme
dchemlett.5b00127
[131] N. Herrera, “Physarella oblonga-centered bioassays for testing the biological activity of myxomycetes”, Mycosphere, vol. 2, n.º 6, pp. 637–644, noviembre de 2011. https://doi.org/10.5943/mycosphere/2/6/4
[132] M. Benavides, E. Hernández, “Análisis espectroscópico del precipitado formado por la mezcla de hipoclorito de sodio y clorhexidina utilizando resonancia magnética nuclear”, International Journal of Dental Sciences, vol. 17, n° 3, pp. 55-60, 2015. Accedido el 10 de enero de 2023. [En línea]. Disponible: https://fodo.ucr.ac
.cr/sites/default/files/revista/Benavides%20M.pdf
[133] B. Matarrita-Carranza et al., “Streptomyces sp. M54: an actinobacteria associated with a neotropical social wasp with high potential for antibiotic production”, Antonie van Leeuwenhoek, vol. 114, n.º 4, pp. 379–398, febrero de 2021. https://doi.
org/10.1007/s10482-021-01520-y
[134] J. A. Solera-Rojas, M. Ledezma-Gairaud y L. W. Pineda, “Síntesis y evaluación de complejos de cobre (I/II) con ligandos pilipiridínicos como mediadores redox en celdas solares sensibilizadas con tintes”, Ciencia y Tecnología, vol. 36, n.º 1, pp. 37-58, febrero de 2020. Accedido el 25 de junio de 2023. [En línea]. Disponible: https://revistas.ucr.ac.cr/index.php/cienciaytecnologia/article/view/43602
[135] C. Murillo, F. J. Albertazzi, J. Carranza, H. T. Lumbsch y G. Tamayo, “Molecular data indicate that Rhytidhysteron rufulum (ascomycetes, Patellariales) in Costa Rica consists of four distinct lineages corroborated by morphological and chemical characters”, Mycolog. Res., vol. 113, n.º 4, pp. 405–416, abril de 2009. https://doi.org/10.1016/j.mycres.2008.09.003
[136] M. Navarro-Hoyos et al., “Proanthocyanidin Characterization and Bioactivity of Extracts from Different Parts of Uncaria tomentosa L. (Cat’s Claw)”, Antioxidants, vol. 6, n.º 1, p. 12, febrero de 2017. https://doi.org/10.3390/antiox6010012
[137] G. Petschenka, C. S. Fei, J. J. Araya, S. Schröder, B. N. Timmermann y A. A. Agrawal, “Relative Selectivity of Plant Cardenolides for Na+/K+-ATPases From the Monarch Butterfly and Non-resistant Insects”, Frontiers Plant Sci., vol. 9, septiembre de 2018. https://doi.org/10.3389/fpls.2018.01424
[138] R. Murillo, V. Castro, J. Araya y L. Poveda, “Nuevas Lactonas Sesquiterpénicas de Perymenium grande”, Ciencia y Tecnología, vol. 24, n.º 2, diciembre de 2006. Accedido el 5 de julio de 2023. [En línea]. Disponible: https://revistas.ucr.ac.cr/ind
ex.php/cienciaytecnologia/article/view/2648/2599
[139] T. D. Locklear et al., “Estrogenic and progestagenic effects of extracts of Justicia pectoralis Jacq., an herbal medicine from Costa Rica used for the treatment of menopause and PMS”, Maturitas, vol. 66, n.º 3, p. 315–322, julio de 2010. https://doi.org/10.1016/j.maturitas.2010.04.001
[140] Y. Carvajal-Miranda, R. Pérez-Salazar y J. A. Varela, “Synthesis of Dihydroindolo[2,3-c]carbazole as Potential Telomerase Inhibitor”, J. Heterocyclic Chemistry, vol. 53, n.º 3, pp. 762–766, mayo de 2015. https://doi.org/10.1002/jhet.2333
[141] J. R. Villegas, M. Calvo, I. Castro-Gamboa y O. Castro, “Identificación de lignanas en hojas de Rollinia mucosa (JACQ) Bail.annonaceae”, Uniciencia, vol. 18, n.º 1, pp. 39-42, 2001. Accedido el 7 de julio de 2023. [En línea]. Disponible: https://repositorio.una.ac.cr/bitstream/handle/11056/25196/Vol%2018%20No%201%202001.%205.pdf?sequence=1&isAllowed=y
[142] E. Ballestero-Martínez, J. T. Ferguson, M. A. Siegler y R. S. Klausen, “Isolation of a Cyclopentasilane from Magnesium Reduction of a Linear Hexasilane”, Eur. J. Organic Chemistry, vol. 2021, n.º 33, pp. 4641–4646, septiembre de 2021. https://doi.org/10.1002/ejoc.202100768
[143] J. P. de Andrade et al., “Crinine-type alkaloids from Hippeastrum aulicum and H. calyptratum”, Phytochemistry, vol. 103, pp. 188–195, julio de 2014. https://doi.or
g/10.1016/j.phytochem.2014.03.007
[144] L. M. C. Cursino, N. M. Lima, R. Murillo, C. V. Nunez, I. Merfort y M. Humar, “Isolation of Flavonoids from Deguelia duckeana and Their Effect on Cellular Viability, AMPK, eEF2, eIF2 and eIF4E”, Molecules, vol. 21, n.º 2, p. 192, febrero de 2016. https://doi.org/10.3390/molecules21020192
[145] L. Gómez-Rodríguez, P. J. Schultz, G. Tamayo-Castillo, G. D. Dotson, D. H. Sherman y A. Tripathi, “Adipostatins E-J, new potent antimicrobials identified as inhibitors of coenzyme-A biosynthesis”, Tetrahedron Letters, vol. 61, n.º 5, pp. 151-469, enero de 2020. https://doi.org/10.1016/j.tetlet.2019.151469
[146] S. R. Park et al., “Discovery of cahuitamycins as biofilm inhibitors derived from a convergent biosynthetic pathway”, Nature Communications, vol. 7, n.º 1, febrero de 2016. https://doi.org/10.1038/ncomms10710
[147] L. A. Mike et al., “Discovery of nicoyamycin A, an inhibitor of uropathogenic Escherichia coli growth in low iron environments”, Chemical Communications, vol. 53, n.º 95, pp. 12778–12781, 2017. https://doi.org/10.1039/c7cc07732g
[148] C. De Ford et al., “Discovery of Tricyclic Clerodane Diterpenes as Sarco/Endoplasmic Reticulum Ca2+-ATPase Inhibitors and Structu- re–Activity Relationships”, Journal of Natural Products, vol. 78, n.º 6, pp. 1262–1270, mayo de 2015. https://doi.org/10
.1021/acs.jnatprod.5b00062
[149] J. L. Michel et al., “Estrogenic and serotonergic butenolides from the leaves of Piper hispidum Swingle (Piperaceae)”, Journal of Ethnopharmacology, vol. 129, n.º 2, pp. 220–226, mayo de 2010. https://doi.org/10.1016/j.jep.2010.03.008
[150] E. B. Van Arnam et al., “Selvamicin, an atypical antifungal polyene from two alternative genomic contexts”, Proceedings of the National Academy of Sciences, vol. 113, n.º 46, pp. 12940–12945, noviembre de 2016. https://doi.org/10.1073/p
nas.1613285113
[151] P. M. García-Barrantes, G. V. Lamoureux, A. L. Pérez, R. N. García-Sánchez, A. R. Martínez y A. San Feliciano, “Synthesis and biological evaluation of novel ferrocene–naphthoquinones as antiplasmodial agents”, European Journal of Medicinal Chemistry, vol. 70, pp. 548–557, diciembre de 2013. https://doi.org/10.1016/j.ejm
ech.2013.10.011
[152] H. Achenbach, U. Hefter-Bübl y M. A. Constenla, “Fevicordin A and fevicordin A glucoside, novel norcucurbitacins from Fevillea cordifolia”, J. Chem. Soc., Chem. Commun., n.º 6, pp. 441–442, 1987. https://doi.org/10.1039/c39870000441
[153] C. G. Guerrieri et al., “Alkaloids from Crinum erubescens Aiton”, Arabian J. Chem., vol. 9, n.º 5, pp. 688–693, septiembre de 2016. https://doi.org/10.1016/j.arab
jc.2015.07.009
[154] C. Calderón, C. De Ford, V. Castro, I. Merfort y R. Murillo, “Cytotoxic Clerodane Diterpenes from Zuelania guidonia”, J. Natural Products, vol. 77, n.º 3, pp. 455–463, enero de 2014. https://doi.org/10.1021/np400672g
[155] B. J. Doyle et al., “Isolation and identification of three new chromones from the leaves of Pimenta dioica with cytotoxic, oestrogenic and anti-oestrogenic effects”, Pharmaceutical Biol., vol. 56, n.º 1, pp. 235–244, enero de 2018. https://doi.org/1
0.1080/13880209.2018.1448873
[156] C. A. K. Ta et al., “Antifungal Saponins from the Maya Medicinal PlantCestrum schlechtendahliiG. Don (Solanaceae)”, Phytotherapy Res., vol. 30, n.º 3, pp. 439–446, diciembre de 2015. https://doi.org/10.1002/ptr.5545
[157] C. Nicolaus, A. Sievers-Engler, R. Murillo, M. D’Ambrosio, M. Lämmerhofer y I. Merfort, “Mastering analytical challenges for the characterization of pentacyclic triterpene mono- and diesters of Calendula officinalis flowers by non-aqueous C30 HPLC and hyphenation with APCI-QTOF-MS”, Journal of Pharmaceutical and Biomedical Analysis, vol. 118, pp. 195–205, enero de 2016. https://doi.org
/10.1016/j.jpba.2015.10.025
[158] O. Castro, J. M. Gutiérrez, M. Barrios, I. Castro, M. Romero y E. Umaña, “Neutralización del efecto hemorrágico inducido por veneno de Bothrops asper (Serpientes: Viperidae) por extractos de plantas tropicales”, Revista de Biología Tropical, vol. 47, pp. 605-616, 1999. Accedido el 25 de junio de 2023. [En línea]. Disponible: https://www.kerwa.ucr.ac.cr/bitstream/handle/10669/25752/157_19
99_RevBiolTrop_Castro_%20Plants_venom_hemorrhage.pdf?sequence=1&isAllowed=y
[159] B. Garita-Salazar y L. W. Pineda, “1,3-Bis[(2,6-dimethylphenyl)sulfanyl]methylbenz ene”, IUCrData, vol. 4, n.º 5, mayo de 2019. https://doi.org/10.1107/s241431461
9006771
[160] C. Steinbrueck, N. Mora-Ugalde, C. Morales, R. Loiaza, A. J. García-Piñeres y J. J. Araya, “Bioassay-guided isolation of anti-inflammatory O-sulfated withanolides from Acnistus arborescens (Solanaceae)”, Phytochemistry Letters, vol. 29, pp. 190–194, febrero de 2019. https://doi.org/10.1016/j.phytol.2018.12.001
[161] S. Lee, G. Tamayo-Castillo, C. Pang, J. Clardy, S. Cao y K. H. Kim, “Diketopiperazines from Costa Rican endolichenic fungus Colpoma sp. CR1465A”, Bioorganic & Medicinal Chemistry Letters, vol. 26, n.º 10, pp. 2438–2441, mayo de 2016. https://doi.org/10.1016/j.bmcl.2016.03.115
[162] V. Núñez, V. Castro, R. Murillo, L. A. Ponce-Soto, I. Merfort y B. Lomonte, “Inhibitory effects of Piper umbellatum and Piper peltatum extracts towards myotoxic phospholipases A2 from Bothrops snake venoms: Isolation of 4-nerolidylcatechol as active principle”, Phytochemistry, vol. 66, n.º 9, pp. 1017–1025, mayo de 2005. https://doi.org/10.1016/j.phytochem.2005.03.026
[163] R. Murillo, V. Castro, M. Chavarría y L. Poveda, “Lignanos de Zanthoxylum acuminatum”, Revista de Ciencia y Tecnología, vol. 24, n.º 2, enero de 2009. Accedido el 10 de enero de 2023. [En línea]. Disponible: https://revistas.ucr.ac.cr/index.php/cienciaytecnologia/article/view/2649/2600
[164] J. Parra, et al., “Phytochemical characterization and antioxidant profile of Sechiumedule (Jacq) Swartz Cucurbitaceae) varieties grown in Costa Rica”, Journal of Pharmacy and Pharmacognosy Research, vol. 6, n.º 6, pp. 448-457, 2018. Accedido el 10 de enero de 2023. [En línea]. Disponible: https://jppres.com/jppr
es/pdf/vol6/jppres18.379_6.6.448.pdf
[165] J. J. Araya, K. Kindscher y B. N. Timmermann, “Sullivantosides A-F: Pregnane glycosides from Asclepias sullivantii L.”, Phytochemistry Letters, vol. 16, pp. 185–191, junio de 2016. https://doi.org/10.1016/j.phytol.2016.04. 011
[166] M. G. Chevrette et al., “The antimicrobial potential of Streptomyces from insect microbiomes”, Nature Communications, vol. 10, n.º 1, enero de 2019. https://doi.org/10.1038/s41467-019-08438-0
[167] J. Parra, C. D. Ford y R. Murillo, “Phytochemical study of endemic costa rican annonaceae species Annona pittieri and Cymbopetalum costaricense”, J. Chilean Chem. Soc., vol. 66, n.º 1, pp. 5047–5050, enero de 2021. https://doi.org/10.406
7/s0717-97072021000105047
[168] D. Rojas-Azofeifa et al., “Biochemical characterization of the venom of Central American scorpion Didymocentrus krausi Francke, 1978 (Diplocentridae) and its toxic effects in vivo and in vitro”, Comparative Biochemistry Physiol. Part C: Toxicol. & Pharmacol., vol. 217, pp. 54–67, marzo de 2019. https://doi.org/10.1016/j.cb
pc.2018.11.021
[169] J.C. Fuentes, V. Castro, J. Jakupovic y R. Murillo, “Diterpenos y otros constituyentes de Croton hirtus (Euphorbiaceae)”, Rev. Biol. Trop., vol. 52, n.º 1, pp. 269-285, agosto de 2003. Accedido el 2 de julio de 2023. [En línea]. Disponible: https://revistas.ucr.ac.cr/index.php/rbt/article/view/14943/14209
[170] G. V. Perez y A. L. Perez, “Organic Acids without a Carboxylic Acid Functional Group”, Journal of Chemical Education, vol. 77, n.º 7, p. 910, julio de 2000. https://doi.
org/10.1021/ed077p910
[171] G. Lamoureux, A. L. Perez, M. Araya y C. Agüero, “Reactivity and structure of derivatives of 2-hydroxy-1,4-naphthoquinone (lawsone)”, Journal of Physical Organic Chemistry, vol. 21, n.º 12, pp. 1022–1028, diciembre de 2008. https://doi.org/10.1002/poc.1435
[172] A. L. Perez, G. Lamoureux y B. Y. Zhen-Wu, “Synthesis of 2-hydroxy-3-substituted naphthoquinones using the Heck reaction”, Tetrahedron Letters, vol. 48, n.º 23, pp. 3995–3998, junio de 2007. https://doi.org/10.1016/j.tetlet. 2007.04.033
[173] E. B. Camargo-Cortés, M. Acosta, J. C. Martínez y L. W. Pineda, “Tetraaquabis(2,3-dihydro-1,4-benzodioxine-2-carboxylato)calcium(II)”, IUCrData, vol. 5, n.º 8, agosto de 2020. https://doi.org/10.1107/s2414314620010925
[174] C. Machado Fernandes et al., “Use of a theoretical prediction method and quantum chemical calculations for the design, synthesis and experimental evaluation of three green corrosion inhibitors for mild steel”, Colloids and Surfaces A: Physicochemical and Engineering Aspects, vol. 599, p. 124857, agosto de 2020. https://doi.org/10
.1016/j.colsurfa.2020.124857
[175] P. P. Guerra-García y G. Valle-Borrouet, “Síntesis y caracterización del Ligando tris–(2–tiosalicilamidoetil)amina y sus complejos de hierro e indio”, Ciencia y Tecnología vol. 24, pp. 233-241, diciembre de 2006. Accedido el 25 de junio de 2023. [En línea]. Disponible: https://www.kerwa.ucr.ac.cr/bitstream/handle/10669/14626/2650-4130-1-PB.pdf?sequence=1&isAllowed=y
[176] J. Chavarría-Sánchez, C. Herrera Ramírez y G. Lutz, “Caracterización y determinación el potencial aterogénico de quesos producidos en Costa Rica”, Ciencia y Tecnología, vol. 24, n.º 1, pp. 31-50, abril de 2006. Accedido el 25 de junio de 2023. [En línea]. Disponible: Https://revistas.ucr.ac.cr/index.php/cienciaytecnologia/article/view/26
53
[177] M. A. Goetz et al., “Potent nor-triterpenoid blockers of the voltage-gated potassium channel Kv1.3 from Spachea correae”, Tetrahedron Lett., vol. 39, n.º 19, pp. 2895–2898, mayo de 1998. https://doi.org/10.1016/s0040-4039(98)00427-4
[178] M. Navarro, W. Zamora, S. Quesada, G. Azofeifa, D. Alvarado y M. Monagas, “Fractioning of Proanthocyanidins of Uncaria tomentosa. Composition and Structure-Bioactivity Relationship”, Antioxidants, vol. 6, n.º 3, p. 60, julio de 2017. https://doi.org/10.3390/antiox6030060
[179] M. Benavides, E. Hernández y V. Soto-Tellini, “Análisis espectroscópico del precipitado formado por la mezcla de hipoclorito de sodio y clorhexidina utilizando resonancia magnética nuclear”, International Journal of Dental Sciences, vol. 17, n.º 3, pp. 55-60, noviembre de 2015. http://dx.doi.org/10.15517/ijds.v0i0.22146
[180] G. O. Lobitz, G. Tamayo-Castillo y I. Merfort, “Diterpenes and sesquiterpenes from Mikania banisteriae”, Phytochemistry, vol. 46, n.º 1, pp. 161–164, septiembre de 1997. https://doi.org/10.1016/s0031-9422(97)00228-8
[181] G. O. Lobitz, G. Tamayo-Castillo, L. Poveda y I. Merfort, “Kaurene diterpenes from Mikania vitifolia”, Phytochemistry, vol. 49, n.º 3, pp. 805–809, octubre de 1998. https://doi.org/10.1016/s0031-9422(97)01013-3
[182] G. Tamayo-Castillo y V. Castro, “Seco-manool and other constituents from Fleischmannia microstemon”, Phytochemistry, vol. 27, n.º 10, pp. 3322–3323, enero de 1988. https://doi.org/10.1016/0031-9422(88)80056-6
[183] V. Castro, G. Tamayo-Castillo y J. Jakupovic, “Sesquiterpene lactones and other constituents from Calea prunifolia and C. Peckii”, Phytochemistry, vol. 28, n.º 9, pp. 2415–2418, enero de 1989. https://doi.org/10.1016/s0031-9422(00)97995-0
[184] P. Rüngeler, V. Brecht, G. Tamayo-Castillo y I. Merfort, “Germacranolides from Mikania guaco”, Phytochemistry, vol. 56, n.º 5, pp. 475–489, marzo de 2001. https://doi.org/10.1016/s0031-9422(00)00394-0
[185] G. Tamayo-Castillo, J. Jakupovic, F. Bohlmann y V. Castro, “Heliangolides from Viguiera sylvatica”, Phytochemistry, vol. 28, n.º 10, pp. 2737–2740, enero de 1989. https://doi.org/10.1016/s0031-9422(00)98079-8
[186] S. Cao et al., “Phenolic compounds as antiangiogenic CMG2 inhibitors from costa rican endophytic fungi”, Bioorganic & Medicinal Chemistry Lett., vol. 22, n.º 18, pp. 5885–5888, septiembre de 2012. https://doi.org/10. 1016/j.bmcl.2012.07.075
[187] E. Ballestero-Martínez, J. Klosin, B. D. Fahlman y L. W. Pineda, “Monomeric Germanium(II) Amides Bearing β-Diketiminato Ligands: Synthesis, Structural Characterization, and Thermal Properties”, Eur. J. Inorganic Chemistry, vol. 2014, n.º 30, pp. 5233–5239, septiembre de 2014. https://doi.org/10.1002/ejic.201402594
[188] G. Tamayo-Castillo et al., “Isolation of Major Components from the Roots of Godmania aesculifolia and Determination of Their Antifungal Activities”, Planta Medica, vol. 79, n.º 18, pp. 1749–1755, diciembre de 2013. https://doi.org/10.1
055/s-0033-1351025
[189] K. H. Kim et al., “Naphthalenones and Isocoumarins from a Costa Rican Fungus Xylariaceae sp. CR1546C”, J. Chem. Res., vol. 38, n.º 12, pp. 722–725, diciembre de 2014. https://doi.org/10.3184/174751914x14175406270662
[190] G. Tamayo-Castillo, J. Jakupovic, F. Bohlmann, V. Castro y R. M. King, “Ent-clerodane derivatives and other constituents from representatives of the subgenus Ageratina”, Phytochemistry, vol. 28, n.º 1, pp. 139–141, 1989. https://doi.org/10.1016/0031-9422(89)85025-3
[191] S. Cao, D. W. McMillin, G. Tamayo, J. Delmore, C. S. Mitsiades y J. Clardy, “Inhibition of Tumor Cells Interacting with Stromal Cells by Xanthones Isolated from a Costa Rican Penicillium sp.”, J. Natural Products, vol. 75, n.º 4, pp. 793–797, marzo de 2012. https://doi.org/10.1021/np2009863
[192] G. Tamayo-Castillo, J. Jakupovic, F. Bohlmann, A. Rojas, V. Castro y R. M. King, “Germacranolides and other constituents from Ageratina species”, Phytochemistry, vol. 27, n.º 9, pp. 2893–2897, enero de 1988. https://doi.org/10.1016/0031-9422(88)80683-6
[193] R.M. Murillo, J. Jakupovic, J. Rivera y V.H. Castro, “Diterpenes and other constituents from Croton draco (Euphorbiaceae)”, Rev. Biol. Trop., vol. 49, n.º 1, pp. 259-264, julio de 2000. Accedido el 4 de julio de 2023. [En línea]. Disponible: https://revistas.ucr.ac.cr/index.php/rbt/article/view/16917/16379
[194] Á. I. Calderón et al., “Screening of Latin American Plants for Cytotoxic Activity”, Pharmaceutical Biol., vol. 44, n.º 2, pp. 130–140, enero de 2006. https://doi.org/10.1080/13880200600592285
[195] K. Barrantes et al., “Synthesis and Evaluation of Aromatic Surfactants as Potential Antibacterial and Cytotoxic Agents”, Lett. Organic Chemistry, vol. 16, n.º 6, pp. 478–484, abril de 2019. https://doi.org/10.2174/1570178615666181023151308
[196] G. Lamoureux, M. Alvarado-Rojas y L. W. Pineda, “Crystal structure of (E)-2-(tert-butylamino)-4-(tert-butylimino)naphthalen-1(4H)-one”, Acta Crystallographica Sect. E Crystallographic Commun., vol. 74, n.º 7, pp. 973–976, junio de 2018. https://doi.org/10.1107/s2056989018008514
[197] F. A. Vinocour, A. Soto-Navarro y L. W. Pineda, “µ2-Chlorido-chlorido(µ2-4-[2-(diethylamino)ethyl]iminopent-2-en-2-olato)bis(tetrahydrofuran-kO)cobalt(II)lithi um”, IUCrData, vol. 3, n.º 11, noviembre de 2018. https://doi.org/10.1107/s241
4314618015778
[198] M. Chavarría, V. Castro, L. Poveda y R. Murillo, “Cuatro compuestos nuevos del extracto no polar de la planta Amyris brenesii (Rutaceae) de Costa Rica”, Rev. Biol. Trop., vol. 56, n.º 3, septiembre de 2008. Accedido el 6 de julio de 2023. [En línea]. Disponible: https://revistas.ucr.ac.cr/index.php/rbt/article/view/5691/5433
[199] G. Chavarría, F. Granados-Chinchilla, M. Alfaro-Cascante y A. Molina, “Detection of aflatoxin M1 in milk, cheese and sour cream samples from Costa Rica using enzyme-assisted extraction and HPLC”, Food Additives & Contaminants: Part B, vol. 8, n.º 2, pp. 128–135, abril de 2015. https://doi.org/10.1080/19393210.2015.1015176
[200] M. Navarro Hoyos et al., “Phenolic Assesment of Uncaria tomentosa L. (Cat’s Claw): Leaves, Stem, Bark and Wood Extracts”, Molecules, vol. 20, n.º 12, pp. 22703–22717, diciembre de 2015. https://doi.org/10.3390/molecules201219875
[201] S. Mora, V. Castro, L. Poveda, M. Chavarría y R. Murillo, “Two New 3,4-Seco-ent-kaurenes and Other Constituents from the Costa Rican Endemic Species Croton megistocarpus”, Helvetica Chimica Acta, vol. 94, n.º 10, pp. 1888–1892, octubre de 2011. https://doi.org/10.1002/hlca.201100127
[202] K. Wilhelm-Romero et al., “Evaluation of Piperine as Natural Coformer for Eutectics Preparation of Drugs Used in the Treatment of Cardiovascular Diseases”, AAPS PharmSciTech, vol. 23, n.º 5, abril de 2022. https://doi.org/10.1208/s12249-022-02270-4
[203] A. M. Araya-Sibaja et al., “Crystal Forms of the Antihypertensive Drug Irbesartan: A Crystallographic, Spectroscopic, and Hirshfeld Surface Analysis Investigation”, ACS Omega, abril de 2022. https://doi.org/10.1021/acsomega. 2c00545
[204] A. M. Araya-Sibaja et al., “The effect of solution environment and the electrostatic factor on the crystallisation of desmotropes of irbesartan”, RSC Advances, vol. 9, n.º 9, pp. 5244–5250, 2019. https://doi.org/10.1039/c8ra10146a
[205] S. A. Patil et al., “Synthesis, Characterization and Crystal Structure of (2Z)-3-[(4-Methylphenyl)amino]-1-phenylbut-2-en-1-one”, J. Chem. Crystallogr., vol. 42, n.º 6, pp. 560–565, febrero de 2012. https://doi.org/10.1007/s10870-012-0279-8
[206] D. González-Flores et al., “Synthesis of hafnium(IV) β-ketoiminates as potential precursors for the MOCVD of HfO2”, Inorganica Chimica Acta, vol. 396, pp. 60–65, febrero de 2013. https://doi.org/10.1016/j.ica.2012.10.002
[207] S. Mora, V. Castro, L. Poveda, M. Chavarría y R. Murillo, “Chemical constituents from Zanthoxylum setulosum (Rutaceae)”, Boletín Latinoamericano y del Caribe de Plantas Medicinales y Aromáticas, vol. 10, pp. 155-158, marzo de 2011. Accedido el 7 de julio de 2023. [En línea]. Disponible: https://repositorio.una.ac.cr/bitstre
am/handle/11056/25797/85617384009.pdf?sequence=1
[208] C. P. Hasbun, M. Calderon, O. Castro, E. Gács-Baitz, G. Delle Monache y F. Delle Monache, “Maxonine, a novel alkaloid from Simira maxonii”, Tetrahedron Lett., vol. 30, n.º 45, pp. 6199–6202, 1989. https://doi.org/10.1016/s0040-4039(01)93341-6
[209] I. Castro-Gamboa y O. Castro, “Iridoids from the aerial parts of Verbena littoralis (Verbenaceae)”, Phytochemistry, vol. 65, n.º 16, pp. 2369–2372, agosto de 2004. https://doi.org/10.1016/j.phytochem.2004.07.008
[210] M. Cordero et al., “Caracterización química y funcional de metabolitos antimicrobianos aislados de Ascidian rhopalaea birkelandi”, Revista Ciencias Marinas y Costeras, vol. 3, pp. 111-125, diciembre de 2011. https://doi.org/10
.15359/revmar.3.9
[211] D. C. Chauret et al., “Novel steroids from Trichilia hirta as identified by nanoprobe INADEQUATE 2D-NMR spectroscopy”, Tetrahedron Lett., vol. 37, n.º 44, pp. 7875–7878, octubre de 1996. https://doi.org/10.1016/0040-4039(96)01803-5
[212] D. C. Chauret et al., “Insecticidal Neolignans fromPiper decurrens”, J. Natural Products, vol. 59, n.º 2, pp. 152–155, enero de 1996. https://doi.org/10.1021/
np960036y
[213] K. Siems, J. Jakupovic, V. Castro y L. Poveda, “Constituents of two Acalypha species”, Phytochemistry, vol. 41, n.º 3, pp. 851–853, febrero de 1996. https://doi.org/1
0.1016/0031-9422(95)00650-8
[214] S. A. Patil et al., “Synthesis, Characterization and Crystal Structure of (Z)-3-(4-Chlorophenylamino)-1-Phenylbut-2-En-1-One”, J. Chem. Crystallogr., vol. 42, n.º 6, pp. 543–548, febrero de 2012. https://doi.org/10.1007/s10870-012-0276-y
[215] J. Cabezas, R. Poveda y J. Brenes, “One-Pot Conversion of Aldehydes and Ketones into 1-Substituted and 1,4-Disubstituted 1,3-Enynes”, Synthesis, vol. 50, n.º 17, pp. 3307–3321, julio de 2018. https://doi.org/10.1055/s-0037-1610197
[216] J. J. Araya, F. Binns, K. Kindscher y B. N. Timmermann, “Verticillosides A–M: Polyoxygenated pregnane glycosides from Asclepias verticillata L.”, Phytochemistry, vol. 78, pp. 179–189, junio de 2012. https://doi.org/10.1016/j.phytoch
em.2012.02.019
[217] M. Asim, H. Hussien, L. Poveda, J. T. Arnason y T. Durst, “Triterpenoids from the bark of Ruptiliocarpon caracolito”, Phytochemistry, vol. 71, n.º 11-12, pp. 1418–1422, agosto de 2010. https://doi.org/10.1016/j.phytochem. 2010.04.020
[218] C. A. Schmidt, R. Murillo, B. Heinzmann, S. Laufer, V. Wray y I. Merfort, “Structural and Conformational Analysis of Proanthocyanidins fromParapiptadenia rigidaand Their Wound-Healing Properties”, J. Natural Products, vol. 74, n.º 6, pp. 1427–1436, junio de 2011. https://doi.org/10.1021/np200158g
[219] G. Solano, C. A. Motti y M. Jaspars, “New iodotyramine derivatives from Didemnum rubeum”, Tetrahedron, vol. 65, n.º 36, pp. 7482–7486, septiembre de 2009. https://doi.org/10.1016/j.tet.2009.07.002
[220] F. Geller et al., “Four New Flavonol Glycosides from the Leaves of Brugmansia suaveolens”, Molecules, vol. 19, n.º 5, pp. 6727–6736, mayo de 2014. https://doi.org/10.3390/molecules19056727
[221] M. Asim, H. Hussien, J. T. Arnason, L. Poveda y T. Durst, “Spirocaracolitone Triterpenoids from the Bark ofRuptiliocarpon caracolito”, J. Natural Products, vol. 70, n.º 8, pp. 1228–1232, agosto de 2007. https://doi.org/10.1021/np060490u
[222] T. Soto-Montero et al., “Dopant-Free Hole-Transport Materials with Germanium Compounds Bearing Pseudohalide and Chalcogenide Moieties for Perovskite Solar Cells”, Inorganic Chemistry, vol. 59, n.º 20, pp. 15154–15166, octubre de 2020. https://doi.org/10.1021/acs.inorgchem.0c02120
[223] R. Vásquez, N. Rios, G. Solano y L. Cubilla-Rios, “Lentinoids A–D, New Natural Products Isolated from Lentinus strigellus”, Molecules, vol. 23, n.º 4, p. 773, marzo de 2018. https://doi.org/10.3390/molecules23040773
[224] A. Tripathi et al., “Baulamycins A and B, Broad-Spectrum Antibiotics Identified as Inhibitors of Siderophore Biosynthesis in Staphylococcus aureus and Bacillus anthracis”, J. Amer. Chem. Soc., vol. 136, n.º 4, pp. 1579–1586, enero de 2014. https://doi.org/10.1021/ja4115924
[225] M. Fronza et al., “In vitro cytotoxic activity of abietane diterpenes from Peltodon longipes as well as Salvia miltiorrhiza and Salvia sahendica”, Bioorganic & Medicinal Chemistry, vol. 19, n.º 16, pp. 4876–4881, agosto de 2011. https://doi.org/10.1
016/j.bmc.2011.06.067
[226] S. Arce-Solano y E. Hernández-Carvajal, “Implementación de las técnicas de RMN y cristalografía de macromoléculas para la caracterización estructural de proteínas de interés biomédico”, Revista Tecnología en Marcha, septiembre de 2019. https://doi.org/10.18845/tm.v32i9.4627
[227] G. P. Barletta, M. Barletta, T. E. Saldaño y S. Fernandez-Alberti, “Analysis of changes of cavity volumes in predefined directions of protein motions and cavity flexibility”, J. Comput. Chemistry, vol. 43, n.º 6, pp. 391–401, diciembre de 2021. https://doi.org/10.1002/jcc.26799
[228] A. Puente-Urbina, J. Hollenbach, I. F. Céspedes-Camacho, J. Matysik y G. Valle-Bourrouet, “Effect of pretreatment temperature on the surface modification of diatomite with trimethylchlorosilane”, J. Porous Mater., vol. 23, n.º 6, pp. 1439–1449, junio de 2016. https://doi.org/10.1007/s10934-016-0204-1
[229] J. D. Barboza-Carmona, M. Wenzel, L. Eckert, D. Enke, J. Matysik y I. F. Céspedes-Camacho, “A spectroscopic insight of the porous structure of hydrophobic silica aerogels by hyperpolarized 129Xe NMR”, J. Sol-Gel Sci. Technol., vol. 101, n.º 1, pp. 176–184, noviembre de 2021. https://doi.org/10.1007/s10971-021-05684-x
[230] C. Fandaruff et al., “Polymorphism of Anti-HIV Drug Efavirenz: Investigations on Thermodynamic and Dissolution Properties”, Cryst. Growth & Des., vol. 14, n.º 10, pp. 4968–4975, septiembre de 2014. https://doi.org/10.1021/cg500509c
[231] S. González-Montiel et al., “Experimental and theoretical studies of C–H-M interactions in palladium and platinum complexes derived from 1,2-bis-(2-hydroxymethylphenylthio)ethane”, Polyhedron, vol. 87, pp. 181–193, febrero de 2015. https://doi.org/10.1016/j.poly.2014.11.007
[232] J. Antony, E. Hardy y N. Nestle, “Low-field NMR methods applied to the characterization of coconut cream”, Revista de Ciencia y Tecnología, vol. 31, n° 1, 2015. Accedido el 10 de enero de 2023. [En línea]. Disponible: https://revistas.ucr.ac.cr/index.php/cienciaytecnologia/article/view/24918/25124
[233] A. Montoya-Arroyo, C. Díaz, F. Vaillant y G. Tamayo-Castillo, “Oral administration of Costa Rican guava (Psidium friedrichsthalianum) juice induces changes in urinary excretion of energy-related compounds in Wistar rats determined by 1H NMR”, NFS Journal, vol. 20, pp. 48–57, agosto de 2020. https://doi.org/10.1016/j.nfs.202
0.07.003
[234] L. Rojas et al., “Simple route for nano-hydroxyapatite properties expansion”, Biomed. Mater., vol. 10, n.º 5, p. 055015, octubre de 2015. https://doi.org/10.108
8/1748-6041/10/5/055015
[235] C. Nicolaus, S. Junghanns, A. Hartmann, R. Murillo, M. Ganzera y I. Merfort, “In vitro studies to evaluate the wound healing properties of Calendula officinalis extracts”, J. Ethnopharmacol., vol. 196, pp. 94–103, enero de 2017. https://doi.org/10.10
16/j.jep.2016.12.006
[236] D. Gräsing et al., “Field-cycling NMR with high-resolution detection under magic-angle spinning: determination of field-window for nuclear hyperpolarization in a photosynthetic reaction center”, Scientific Rep., vol. 7, n.º 1, septiembre de 2017. https://doi.org/10.1038/s41598-017-10413-y
[237] R. González-Paz, V. Cádiz, R. Kiara y J. Vega-Baudrit, “Isomerization of Fatty Acids: A Cellular Barrier Mechanism in Nanotechnology?”, J. Nanosci. Nanotechnol., vol. 17, n.º 8, pp. 5436–5444, agosto de 2017. https://doi.org/10.1166/jnn.2017.13791
[238] G. Torrentes-Espinoza, B. C. Miranda, J. Vega-Baudrit y J. F. Mata-Segreda, “Castor oil (Ricinus communis) supercritical methanolysis”, Energy, vol. 140, pp. 426–435, diciembre de 2017. https://doi.org/10.1016/j.energy. 2017.08.122
[239] F. J. Benavides Murillo, “Computer simulation of NMR logging”, 2019 IV Jornadas Costarricenses de Investigación en Computación e Informática (JoCICI), San Pedro, Costa Rica, 19–20 de agosto de 2019. IEEE, 2019. https://doi.org/10.1109/jocici483
95.2019.9105319
[240] A. G. Vincent, J. Schleucher, R. Giesler y D. A. Wardle, “Soil phosphorus forms show only minor changes across a 5000-year-old boreal wildfire chronosequence”, Biogeochemistry, febrero de 2022. https://doi.org/10.1007/s10533-022-00910-2
[241] C. V. Corrales et al., “Physicochemical characterization of jicaro seeds ( Crescentia alata H.B.K.): A novel protein and oleaginous seed”, J. Food Composition Anal., vol. 56, pp. 84–92, marzo de 2017. https://doi.org/10.1016/j.jfca.2016.11.007
[242] J. Quesada-Espinoza y R. Murillo-Masís, “Control de calidad de fitofármacos con la utilización de Resonancia Magnética Nuclear (RMN) y la aplicación del análisis de componentes principales (PCA)”, Revista Tecnología en Marcha, octubre de 2019. https://doi.org/10.18845/tm.v32i4.4794
[243] G. Solano, D. Rojas-Gätjens, K. Rojas-Jimenez, M. Chavarría y R. M. Romero, “Biodegradation of plastics at home composting conditions”, Environmental Challenges, vol. 7, p. 100500, abril de 2022. https://doi.org/10.1016/j.e
nvc.2022.100500
[244] G. Solano, “Uso de la resonancia magnética nuclear para la determinación de curcuminoides en cúrcuma y curry producidos y vendidos en Costa Rica”, Ciencia y Tecnología, vol. 29, n.°1, 2013. Accedido el 10 de enero de 2023. [En línea]. Disponible: https://revistas.ucr.ac.cr/index.php/cienciaytecnologia/article/view/1
5208
[245] R. H. Hallett et al., “Aggregation pheromone of coconut rhinoceros beetle,Oryctes rhinoceros (L.) (coleoptera: Scarabaeidae)”, Journal of Chemical Ecology, vol. 21, n.º 10, pp. 1549–1570, octubre de 1995. https://doi.org/10.1007/bf02035152
[246] J. J. Araya y M. Chavarría, Ejercicios de Espectroscopía. 1a ed, San Pedro, Costa Rica: Editorial UCR, 2009.
[247] P. Blanco-Picado, “Posgrado en Química promueve especialización en Resonancia Magnética Nuclear en estado sólido”, Universidad de Costa Rica, 13 de noviembre de 2017. Accedido el 6 de agosto de 2023, [En línea]. Disponible: https://www.ucr.ac.cr/noticias/2017/11/13/posgrado-en-quimica-promueve-esp
ecializacion-en-resonancia-magnetica-nuclear-en-estado-solido.html
[248] The World Bank. “Research and development expenditure (% of GDP) - Costa Rica”. World Bank Open Data. https://data.worldbank.org/indicator/GB.XPD.RSDV.GD.ZS
?locations=CR (accedido el 9 de agosto de 2023).
[249] OECD. “Research and development (R&D) - Gross domestic spending on R&D - OECD Data”. The OECD data. https://data.oecd.org/rd/gross-domestic-spending-on-r-d.htm#indicator-chart (accedido el 9 de agosto de 2023).
[250] N. Chinchilla-Bravo, “Curso de alto nivel sobre Resonancia Magnética Nuclear amplió el conocimiento a estudiante y profesor del TEC para proyecto”, Hoy en el TEC, 05 de abril del 2018. Accedido el 9 de agosto de 2023, [En línea]. Disponible en: https://www.tec.ac.cr/hoyeneltec/2018/04/05/curso-alto-nivel-resonancia-magn
etica-nuclear-amplio-conocimiento-estudiante-profesor-tec
[251] N. Chinchilla-Bravo, “Estudiante recibió capacitación en México sobre Resonancia Magnética Nuclear”, Hoy en el TEC, 07 de agosto de 2023. Accedido el 9 de agosto de 2023, [En línea]. Disponible: https://www.tec.ac.cr/hoyeneltec/2023
/08/07/estudiante-recibio-capacitacion-mexico-resonancia-magnetica-nuclear
[252] N. Chinchilla-Bravo, “Estudiante del TEC realizó pasantía en Alemania sobre fenómenos de relajación en Resonancia Magnética Nuclear”, Hoy en el TEC, 13 de abril de 2023. Accedido el 9 de agosto de 2023, [En línea]. Disponible: https://www.tec.ac.cr/hoyeneltec/2023/04/13/estudiante-tec-realizo-pasantia-ale
mania-fenomenos-relajacion-resonancia-magnetica
1 Escuela de Física, Instituto Tecnológico de Costa Rica, Cartago, Costa Rica.Centro de Investigación y de Servicios Químicos y Microbiológicos (CEQIATEC) Escuela de Química, Instituto Tecnológico de Costa Rica, Costa Rica.
 jose.borloz@gmail.com
jose.borloz@gmail.com  https://orcid.org/0009-0004-9357-3621
https://orcid.org/0009-0004-9357-36212 Escuela de Química, Instituto Tecnológico de Costa Rica, Cartago, Costa Rica. Centro de Investigación y de Servicios Químicos y Microbiológicos (CEQIATEC) Escuela de Química, Instituto Tecnológico de Costa Rica, Costa Rica.
 icespedes@tec.ac.cr
icespedes@tec.ac.cr  https://orcid.org/0000-0003-1514-1343
https://orcid.org/0000-0003-1514-1343