Estudio de materiales arcillosos ricos en óxidos de hierro para la desulfuración de biogás
Study of clay materials rich in iron oxides for the desulfurization of biogas
Fiorella Ulloa-Solano1, Marco Chaves-Flores2, Luis Andres Urvina-Savelli3, Claudia C. Villarreal4
Ulloa-Solano, F; Chaves-Flores, M; Urvina-Savelli, L.A; Villarreal, C.C. Estudio de materiales arcillosos ricos en óxidos de hierro para la desulfuración de biogás . Tecnología en Marcha. Vol. 35, especial Programa de Investigación en Energías Limpias. Julio, 2022. Pág. 94-105. https://doi.org/10.18845/tm.v35i7.6338
https://doi.org/10.18845/tm.v35i7.6338
Palabras clave
Arcillas; limpieza de biogás; desulfuración; biodigestión anaerobia; óxidos de hierro; biorrefinación.
Resumen
Costa Rica podría generar 1,000,000 m3 de metano diariamente a partir de biogás, pero su aprovechamiento energético requiere del proceso de desulfuración, cuyos materiales filtrantes tienen elevados costos y no se producen localmente. En este estudio se analizaron sustratos naturales locales ricos en óxidos de hierro, suelos arcillosos (SR) y rocas rojas (RR), para la remoción del H2S del biogás. El desempeño de los medios filtrantes se estudió en un sistema de biodigestión anaerobia instalado en una finca porcina cuya producción diaria de biogás es 20-30 m3, 70% metano. Inicialmente se analizaron 6 muestras mediante Difracción de Rayos-X (XRD) y Fluorescencia de Rayos-X (XRF) para cuantificar los óxidos de hierro (Fe2O3) y se seleccionaron las 2 muestras de RR con mayor porcentaje de Fe2O3, RR2 con 4.8% w/w y RR3 con 7.2% w/w. La caracterización de las RR, antes y después de usarlas como medio filtrante, se realizó mediante Microscopia Electrónica de Barrido (SEM), Espectroscopía de Dispersión de Energía de Rayos-X (EDS), y XRD combinado con el método Rietveld (XRD-Rietveld). Tras la aplicación de las RR en el filtro desulfurizador, se comprobó la absorción superficial de azufre y una disminución de 4.8% wt. a 1.1% wt. de los Fe2O3. Las RR con un tamaño de partícula entre 2.4 y 6.3 mm tienen la capacidad de remover hasta un 28% de H2S. La baja eficiencia de remoción de H2S de las RR sugiere la búsqueda de materiales con mayor cantidad de óxidos de hierro para mejorar el proceso de desulfuración.
Keywords
Clays; biogas cleaning; desulfurization; anaerobic biodigestion; iron oxides; biorefining.
Abstract
Costa Rica could generate 1,000,000 m3 of methane daily from biogas, but its use as energy source requires the application of desulfurization processes, for which the filtering materials are costly and not locally-sourced. The use of natural filtering substrates that are rich in iron oxides, like clay soils (SR) and red rocks (RR), for the removal of H2S from biogas was studied. The performance of the filter materials was tested in an anaerobic biodigestion system installed in a swine farm, with a daily biogas production of 20-30 m3, 70% methane. Six samples were initially analyzed by X-Ray Diffraction (XRD) and X-Ray Fluorescence (XRF) to quantify the iron oxides (Fe2O3) and two RR samples with the highest percentage of Fe2O3 were selected, RR2 with 4.8% w/w and RR3 with 7.2% w/w. The characterization of the filter media, before and after its use as a filter, was carried out using Scanning Electron Microscopy (SEM), X-Ray Energy Dispersion Spectroscopy (EDS), and XRD combined with Rietveld´s method (XRD-Rietveld). The absorption of sulfur was confirmed and a decrease of 4.8% w/w to 1.1% w/w of the Fe2O3 present in the RR was measured in the RR after applying it in the desulfurization process. The RR with a particle size between 2.4- 6.3 mm can remove up to 28% of H2S. The low efficiency of H2S removal suggests the search for other minerals that have higher fraction of iron oxides, to improve the desulfurization efficiency.
Introducción
El biogás es un gas combustible que se produce a partir de reacciones de biodegradación de materia orgánica en un ambiente anaerobio y sus componentes principales son el metano (CH4) y el CO2 [3]. La capacidad calorífica de este gas combustible es cercana a 6 kWh/m3 y depende principalmente de su contenido de CH4 [1], [3]. Al remover el CO2 del biogás, es posible obtener un biocombustible similar al gas natural con una capacidad calorífica cercana a 10 kWh/m3, que lo convierte en una alternativa para la síntesis de combustibles y la generación eléctrica [3], [4]. El CH4 contribuye con más del 20% de los gases de efecto invernadero generados por la sociedad, proveniente principalmente de la agricultura [1]. Al utilizar la capacidad calorífica del CH4 para producir energía, se reducen las emisiones de este gas a la atmósfera, ya que el CH4 tiene el potencial como gas de efecto invernadero (GEI) 23 veces mayor que el dióxido de carbono (CO2), aportando a las acciones de mitigación del cambio climático [2].
Para el uso del biogás como fuente de energía renovable es necesario contar con un control de calidad que garantice un adecuado rendimiento energético, la seguridad de operarios y usuarios de los sistemas de biodigestión, y una prologada vida útil de los sistemas de aprovechamiento. El estudio de procesos para la eliminación de los contaminantes presentes en el biogás (H2S, siloxanos, agua, CO2 y otros) es de gran importancia, debido a los problemas de corrosión y obstrucciones que generan en los sistemas de aprovechamiento, transporte y almacenamiento de biogás [5], [6]. El H2S se produce por la acción de microrganismo anaerobios que tienen la capacidad de reducir sulfatos [5], [7] y cuando entra en contacto con el vapor de agua, se produce el H2SO4, que es un compuesto muy corrosivo para las superficies metálicas [6]. Un control estricto de los procesos de captura de H2S tiene tanto beneficios medioambientales como sociales. Al tratar este gas previo a los procesos de combustión se garantiza un uso seguro para las personas, debido a que el H2S es un compuesto perjudicial para la salud humana y animal, puede provocar mareos, dolor de cabeza, náuseas, irritación de las membranas mucosas y muerte súbita [8] [9]. Además, el biogás es una alternativa para el desarrollo de zonas rurales y de difícil acceso, ya que permite reducir el uso de combustibles tradicionales, como lo son la leña y el estiércol seco que causan problemas de salud asociados a su uso [10].
Algunos de los métodos fisicoquímicos que se utilizan para la remoción de los contaminantes presentes en el biogás son la adsorción y la absorción [5], [6], [9], [11]. Para los procesos de adsorción se emplean materiales como carbón activado, óxidos metálicos y arcillas, mientras que en los procesos de absorción se utilizan cloruro de hierro, hidróxidos diluidos y solventes orgánicos [4]. Los óxidos metálicos permiten la adsorción de H2S mediante la producción de sulfuros. Algunos óxidos metálicos ampliamente utilizados son, hidróxido de hierro (III) (Fe(OH)3) y/o óxido de hierro (III) (Fe2O3) [3]. La reacción de desulfuración con óxidos metálicos se muestra en la ecuación 1, donde M es el catión que genera el sitio activo para la remoción de H2S, los productos de la reacción son sulfuro metálico y H2O [12], [13]. El proceso de regeneración de los óxidos metálicos en presencia de oxígeno está dado por la ecuación 2, donde los productos de la reacción son óxido metálico y azufre elemental [12], [13].
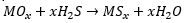 (1)
(1)
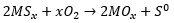 (2)
(2)
La reacción de desulfuración en la superficie de los óxidos metálicos ocurre a través de la interacción de pares de iones o por la interacción en sitios de defecto. Los procesos de desulfuración se llevan a cabo con iones S2- sustituyendo los iones O2- del material original [14]. Los óxidos y oxihidróxidos de hierro presentan una diferencia en el alcance de la reacción, en comparación con otros óxidos metálicos, debido a la diferencia en la fuerza de los enlaces metal-oxígeno, ya que es más baja para enlaces Fe-O, lo que permite una fácil sustitución de iones O2- por iones S2- [14].
Actualmente los materiales ferrosos juegan un papel importante en procesos de desulfuración a baja temperatura y han sido utilizados ampliamente en tratamiento de gases industriales [15]. Algunos factores que pueden influir en el rendimiento del material adsorbente son el tamaño de partícula, la temperatura de calcinación, el área superficial, volumen y tamaño de poro, la cantidad de masa adsorbente, el caudal de biogás, y la capacidad de regeneración del material [9], [11], [15], [16]. Cada una de estas variables puede potenciar o inhibir la capacidad de remoción de H2S en los sustratos filtrantes.
Algunos óxidos de hierro se encuentran de forma natural en suelos y rocas, presentes prácticamente en gran cantidad de minerales. La escoria rojiza es una de las rocas de mayor uso a nivel ornamental, su principal aplicación es la decoración de jardines. También se conocen como bombas rojizas (con presencia de Fe2O3), que en Costa Rica se pueden extraer, de tajos ubicados cerca de los conos piroclásticos de Sabana Redonda de Poás [17]. A pesar de que el porcentaje de óxido de hierro en estos materiales es relativamente bajo, la coloración rojiza que muestran es considerada un indicador de la presencia de óxidos de hierro. La capacidad de remoción de H2S mediante el uso de rocas y suelos rojos reportados por diferentes autores se resumen en el Cuadro 1, donde se evidencia la posibilidad de obtener resultados positivos al usar este tipo de sustratos para disminuir la presencia de H2S en el biogás, y así reducir el impacto de esta traza contaminante en ámbitos socioambientales y económicos.
Cuadro 1. Capacidad de remoción de H2S (experimental) utilizando rocas y suelos rojos.
|
Fuente |
Material |
Sitio activo |
Porcentaje de óxido de hierro |
Capacidad de remoción (g-S/kg) |
|
[5] |
Suelo rojo |
Fe |
14.1-15.5 |
2-12 |
|
[8] |
Suelo rojo |
Fe2O3 |
3.86 3.72 2.76 4.28 |
16.3 16.1 13.1 18.3 |
|
[9] |
Roca roja |
Fe2O3 |
18.81 |
3.5 |
|
[16] |
Lodo rojo (residuos cáusticos) |
Fe2O3 |
30-60 |
21 |
|
[18] |
Suelo rojo |
Fe2O3 |
6.61 |
18.2 |
|
[19] |
Suelo rojo |
Fe2O3 |
6.3 |
18.1 |
Para contribuir con el sector de la biodigestión anaerobia nacional, se estableció como objetivo general de esta investigación el estudio de sustratos filtrantes accesibles a nivel nacional para la desulfuración de biogás. Se analizaron suelos rojos (SR) y rocas rojas (RR) utilizando varias técnicas de caracterización química y se seleccionaron los mejores materiales para ser probados en un biodigestor de 120m3 de una finca porcina. Con este estudio se busca contribuir a prevenir el deterioro de los sistemas de aprovechamiento de biogás y los efectos negativos que el H2S en este biocombustible pueda tener en la salud de las personas y el medio ambiente.
Materiales y métodos
En este estudio se analizaron 3 muestras de suelos rojos (SR) y 3 muestras de rocas rojas (RR). Los SR utilizados en este estudio se recolectaron en la zona de la Miura en Aguacaliente de Cartago, Costa Rica. Los materiales como hojas y raíces de árbol se retiraron de las muestras y estas se secaron a temperatura ambiente durante una semana y luego a 120°C durante 5 horas. En la Figura 1(a) se observan los suelos arcillosos recolectados y en la Figura 1(b) los puntos de muestreo. Las rocas rojas (RR) se adquirieron en el Colono Construcción y en la Ferretería Iztarú, ambos establecimientos se encuentran ubicados en San Rafael de Oreamuno, Cartago, Costa Rica.
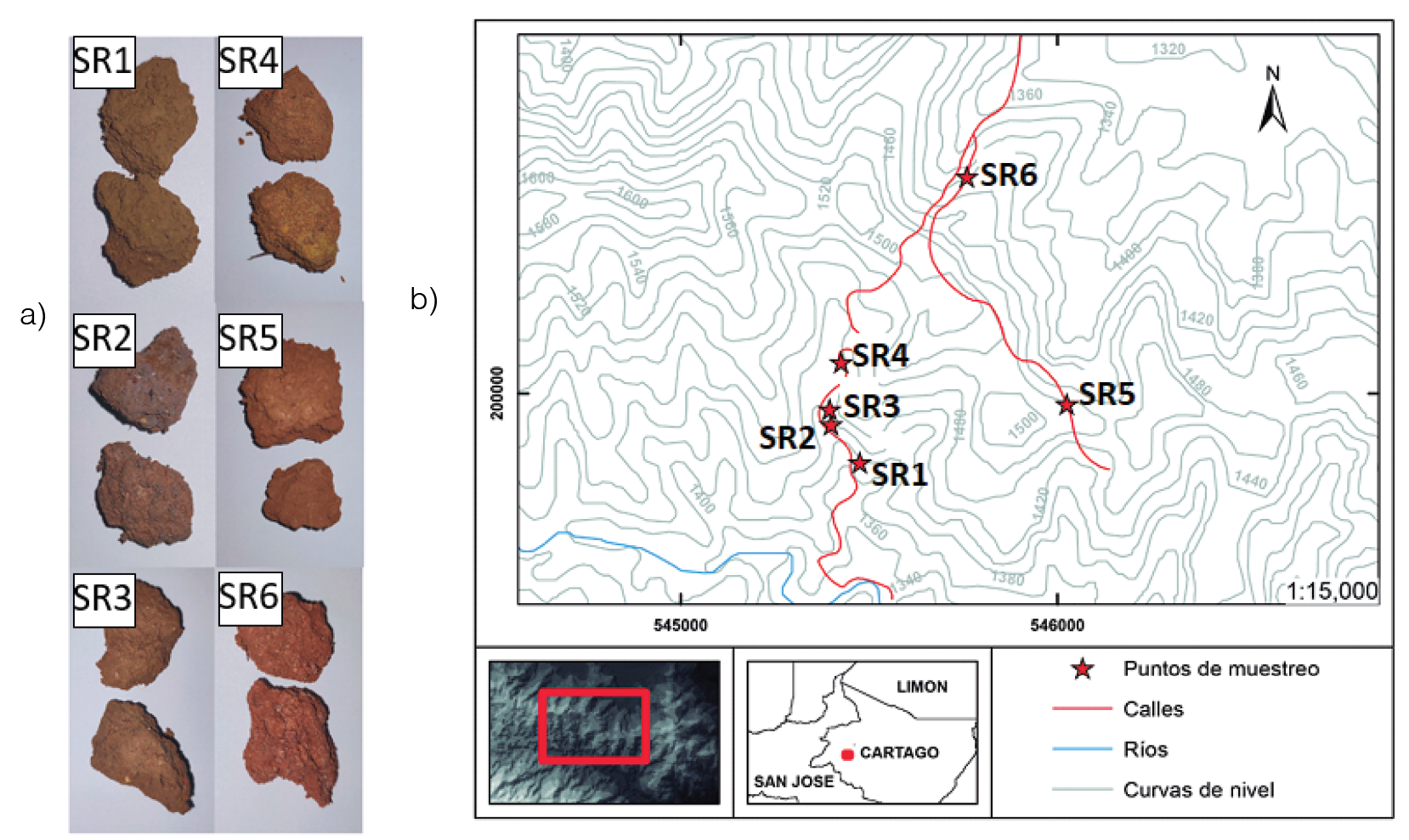
Figura 1. Suelos arcillosos recolectados en la Miura, Aguacaliente de Cartago, Costa Rica. (a) Muestras de SR y (b) Puntos de muestreo.
Inicialmente se seleccionaron los medios filtrantes a colocar en el filtro de desulfuración en base al porcentaje de óxido de hierro, obtenido por medio de Difracción de Rayos-X (XRD) y Fluorescencia de Rayos-X (XRF) de los polvos obtenidos de las muestras. Los difractogtamas se obtuvieron con un difractómetro PANalytical Empyrean escaneo tipo gonio, tubo CuKα (λ=0.154056 nm) que operó a 45 kV y 40 mA, con mediciones de 2q de 10° hasta 70° y una velocidad de paso de 0.013 q/s. Posteriormente se realizó el tratamiento y análisis automático de los difractogramas utilizando el software HighScore Plus. La cuantificación de las fases identificadas se hizo por medio del método desarrollado de Rietveld, usando el programa GSAS-II [20]. Este procedimiento se va a denominar XRD-Rietveld. El porcentaje de hierro en cada muestra se determinó mediante utilizando un analizador de mesa Oxford Lab X-3500.
Las RR con mayor porcentaje de Fe2O3 se utilizaron como medio filtrante tanto con el tamaño de partícula original (RR2-G) como fragmentado en partículas más pequeñas (RR2-P), con el fin de aumentar el área superficial del material en el lecho filtrante. El material se pasó a través de un triturador de mandíbula Denver Equipment modelo “H” del Centro de Investigación en Vivienda y Construcción (CIVCO) del TEC. Después se seleccionó el tamaño de partícula con el uso de tamices con aperturas entre 2.36 mm y 6.3 mm, mediante el uso de la norma ASTM E11-20 [21]. La determinación de porcentaje de absorción en peso de las RR de varias dimensiones se realizó según lo descrito en la norma ASTM designación C97/CM97-09 como se detalla en la ecuación 3, donde M es el peso de la muestra seca y N es el peso de la muestra después de la inmersión [22].
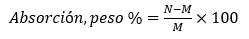 (3)
(3)
El sistema de biodigestión anaerobia utilizado para realizar las pruebas de desempeño de las RR como medios filtrantes se encuentra ubicado en la Finca Los Tejares, 2 km al sur del Aeropuerto Internacional Juan Santamaría (Figura 2(a)). El biodigestor cuenta con una producción estable de biogás de 20-30 m3/día, cuyo contenido de CH4 promedio en de 70% [23]. En la Figura 2(b,c), se muestra la configuración de los filtros y el diagrama esquemático del experimento in situ utilizado para realizar las pruebas de desempeño de las RR. Las mediciones de composición del biogás, temperatura, presión y caudal se realizaron con el equipo Optima Biogas Analyzer de MRU utilizando un puerto hermético en la tubería para obtener mediciones estables y confiables, evitando el ingreso de oxígeno. Las mediciones se realizaron con y sin medio filtrante, cada 5 minutos durante aproximadamente 25 minutos. El rendimiento del material adsorbente denominado “porcentaje de eficiencia de remoción” (RE) se calculó como se muestra en la ecuación 4, donde, C0 y C son las concentraciones de H2S antes y después del paso del biogás a través del filtro [9].
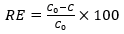 (4)
(4)
(a)
(b)
(c) 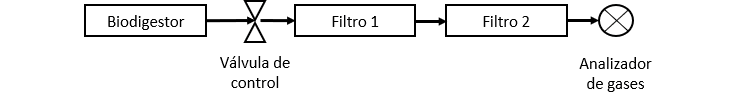
Figura 2. Sistema de biodigestión utilizado para las pruebas de desempeño de los medios filtrantes (a) Biodigestor ubicado en la Finca Los Tejares, Alajuela, Costa Rica, (b) Configuración de los filtros desulfurizadores y (c) Diagrama esquemático del experimento in situ.
Después de las pruebas de desempeño se identificaron y cuantificaron las fases minerales presentes en el sustrato filtrante con el procedimiento XRD-Rietveld. Para el análisis morfológico de la superficie se utilizó un Microscopio Electrónico de Barrido (SEM) Hitachi TM-1000 con un voltaje de aceleración de 15 kV. Las probetas se fijaron al portamuestras con cinta adhesiva de carbono, sin comprometer la región de análisis. La identificación de las especies elementales presentes en la superficie de los sustratos filtrantes se realizó mediante la Espectrometría de Dispersión de Energía de Rayos-X (EDS), utilizando el equipo marca Bruker que se encuentra acoplado al microscopio SEM Hitachi TM-1000, en un ángulo de 22°.
Resultados
Se analizaron piedras y suelos rojos para determinar su potencial como sustratos en filtros desulfurizadores de biogás. Inicialmente se recolectaron 3 muestras de RR y se seleccionaron por inspección visual las 3 muestras de SR con coloración más rojiza. Los SR seleccionados y las RR se analizaron por medio de XRD-Rietveld y XRF para identificar y cuantificar las fases minerales y Fe2O3 presentes. En los SR se identificaron las siguientes fases: óxido de silicio (SiO2), caolinita (Al2Si3O5(OH)4), hematita ((Fe0.008OH0.01)1.136 y Fe2O3) y anatasa (TiO2) (Figura 3(a)) [16]. La presencia de la hematita se identificó debido a los picos ubicados en posiciones 2θ de 33.0°, 35.8° y 39.6° que corresponden a los planos cristalográficos (104), (110) y (006) respectivamente [8]. Para las RR se identificaron las siguientes fases minerales, diopside (Na0.389Ca0.611Mg0.583Ti0.003V0.401Cr0.01Fe0.003Al0.028Si1.972O6), clinoenstatita (Mg(SiO3)), albita (Na(Si3Al)O8) y hematita (Fe2O3) (Figura 3(b)). En las RR se detectaron dos picos para la hematita en posiciones 2θ de 33.2° y 35.7° que se atribuyen a los planos cristalográficos (104) y (110) respectivamente [8]. Tanto para los SR como para las RR, la hematita es la fase activa para la remoción del H2S mientras que las demás fases permiten mejorar la dispersión de los óxidos metálicos que conlleva a un aumento en las posibles colisiones entre el H2S y los Fe2O3 presentes [8].
(a)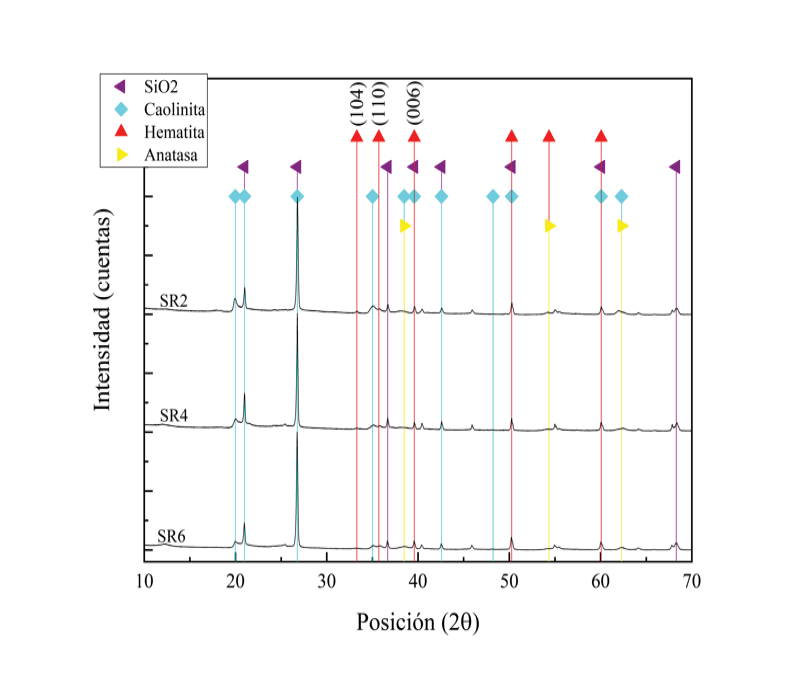 (b)
(b)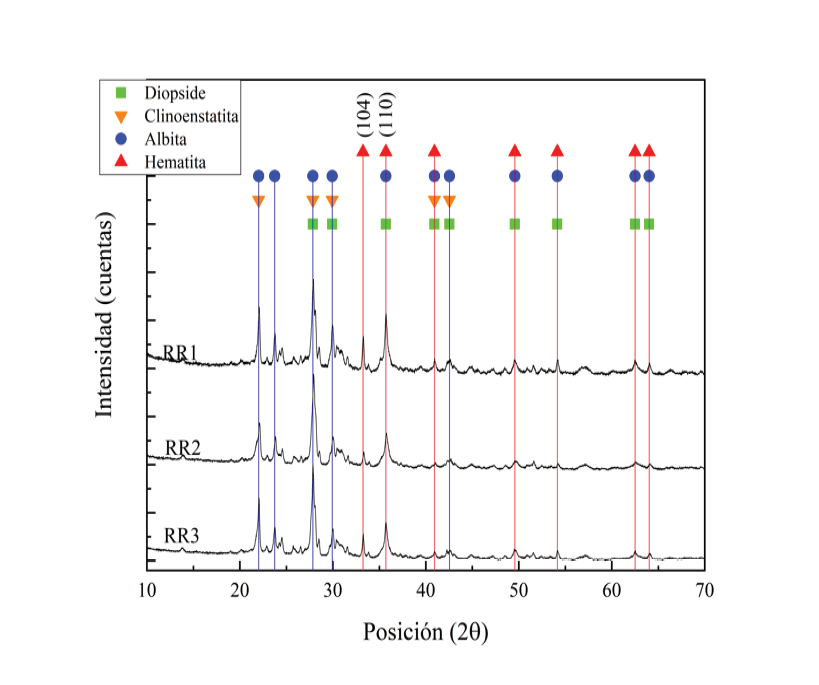
Figura 3. (a) Difractogramas para las muestras de SR originales. (b) Difractogramas para las muestras RR originales.
En el cuadro 1 se muestran los resultados de cuantificación de la hematita (Fe2O3) y del Fe para los SR y RR. Para RR1 se estimó que el porcentaje de Fe2O3 es de 7.2% wt. Al realizar el análisis estequiométrico se obtuvo que la fracción de Fe presente es de 5.0%, similar a lo reportado por el análisis de XRF de 5.195% wt, mientras que el restante 2.2% se atribuye al oxígeno. Algo similar ocurre con RR3, ya que el análisis Rietveld indica que se tiene el mismo porcentaje de Fe2O3. Para RR2 el porcentaje de Fe2O3 es de 4.8% wt, lo que sugiere que su eficiencia de remoción de H2S es menor que para las muestras RR1 y RR3. En cuanto a los SR el porcentaje de hierro obtenido por XRF es más bajo que el reportado para las muestras RR, lo que indica que el porcentaje de Fe2O3 es menor. En base a esta evidencia se decidió usar las RR para el proceso de desulfuración en el sistema de biodigestión anaerobia.
Cuadro 1. Porcentaje de hierro (XRF) y de óxido de hierro (XRD/Rietveld) en los SR y RR seleccionados.
|
Muestra |
RR1 |
RR2 |
RR3 |
SR1 |
SR2 |
SR3 |
|
% wt Fe |
5.950 |
5.173 |
5.195 |
3.015 |
3.922 |
3.346 |
|
% wt Fe2O3 |
7.2 |
4.8 |
7.2 |
- |
- |
- |
Inicialmente se midió la composición química del biogás sin filtrar la cual se muestra en el cuadro 2. La temperatura y presión del sistema durante las mediciones de composición química del biogás se mantuvo estable a 33 °C y 916 hPa, respectivamente. La velocidad de flujo del biogás fue de 3.7 m/s sin filtro y 2.5 m/s con el filtro desulfurizador.
Cuadro 2. Composición media del biogás sin filtrar del sistema de biodigestión anaerobio de la Finca Los Tejares, Alajuela, Costa Rica.
|
Componente |
Concentración |
|
Metano (CH4) |
70.20% |
|
Dióxido de carbono (CO2) |
29.23% |
|
Oxígeno (O2) |
0.0% |
|
Sulfuro de hidrógeno (H2S) |
625 ppm |
En las pruebas de desempeño se compararon RR2 y RR3 (no había disponibilidad del material RR1). Los resultados acerca de la eficiencia de remoción de H2S se muestran en la Figura 4. Inicialmente RR2-G presentó una menor eficiencia de remoción, sin embargo, al llegar a un estado estable supero a RR3, con RE de 20% para RR3 y 23% para RR2-G. Esta discrepancia en la eficiencia de remoción de H2S se atribuye a una posible diferencia en el contenido de óxidos de hierro libres para los dos tipos de RR utilizadas [8], [24]. Es de esperar que RR3 tenga mayor RE por su mayor porcentaje de Fe2O3, pero los resultados fueron lo contrario. La muestra RR2-G se trituró para reducir el tamaño de partícula e incrementar la capacidad de adsorción. El tamaño de partícula se redujo de >6.3mm para RR2-G a un rango de 2.36-6.3 mm para RR2-P, lo que mejoró la eficiencia de remoción de H2S de 23% para RR2-G a 28% para RR2-P, lo cual se puede atribuir a un aumento del área superficial o una mayor exposición de óxidos de hierro libres [8], [24]. Para determinar si el tamaño de partícula es un parámetro determinante en la eficiencia de remoción de H2S mediante el uso de RR, se comparó la capacidad de absorción de agua de ambas muestras RR2-G y RR2-P, utilizando la norma ASTM C97/CM97-09 [17]. El porcentaje de absorción de agua en peso para las RR2-P fue de 11.67% y para las RR2-G el porcentaje de absorción es de 11.11%, lo que evidencia que el tamaño de partícula no es determinante en la mejora del área superficial para la captura del H2S presente en el biogás, ya que probablemente es bastante poroso.
(a)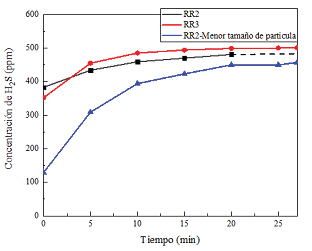 (b)
(b)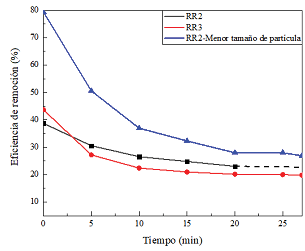
Figura 4. Rendimiento de absorción de la roca roja: (a) Concentración de salida de H2S y (b) Eficiencia de remoción de H2S.
El sustrato RR2-P estuvo 30 días colocado como filtro y expuesto a una corriente de biogás continua, donde sufrió un cambio de color significativo que se observa en la Figura 5(a,b), ya que los óxidos de hierro rojizos se convierten en sulfuro de hierro negro [8], [16], [18]. En la Figura 5(c), se muestra el difractograma de la RR2-P antes y después de ser utilizada como medio filtrante, donde no se identifica ningún componente de azufre. Según la literatura es posible detectar la presencia de pirita de hierro (FeS2) y sulfuro de hierro (II) (FeS) por medio de XRD [8], [16]. Sin embargo, el FeS es sensible al aire y se descompone con facilidad en FeS2 y Fe2O3 a temperatura ambiente, lo que conlleva a pensar que el difractómetro no detectó suficiente FeS. Además, la técnica de XRD tiene baja sensibilidad, ya que solamente es posible detectar fases cristalina cuando estas son mayores a 1%. Al observar con detalle los difractogramas de la Figura 8, se evidencia que el pico en la posición 2θ = 33.2 que se asignó a la hematita presenta una disminución en la intensidad después del proceso de adsorción de H2S [18]. Al cuantificar la hematita por el método XRD/Rietveld se observa una disminución de 4.8 a 1.1 % wt de esta fase tras 30 días de exposición a biogás, que se atribuye a su conversión en FeS, según ecuación 1.
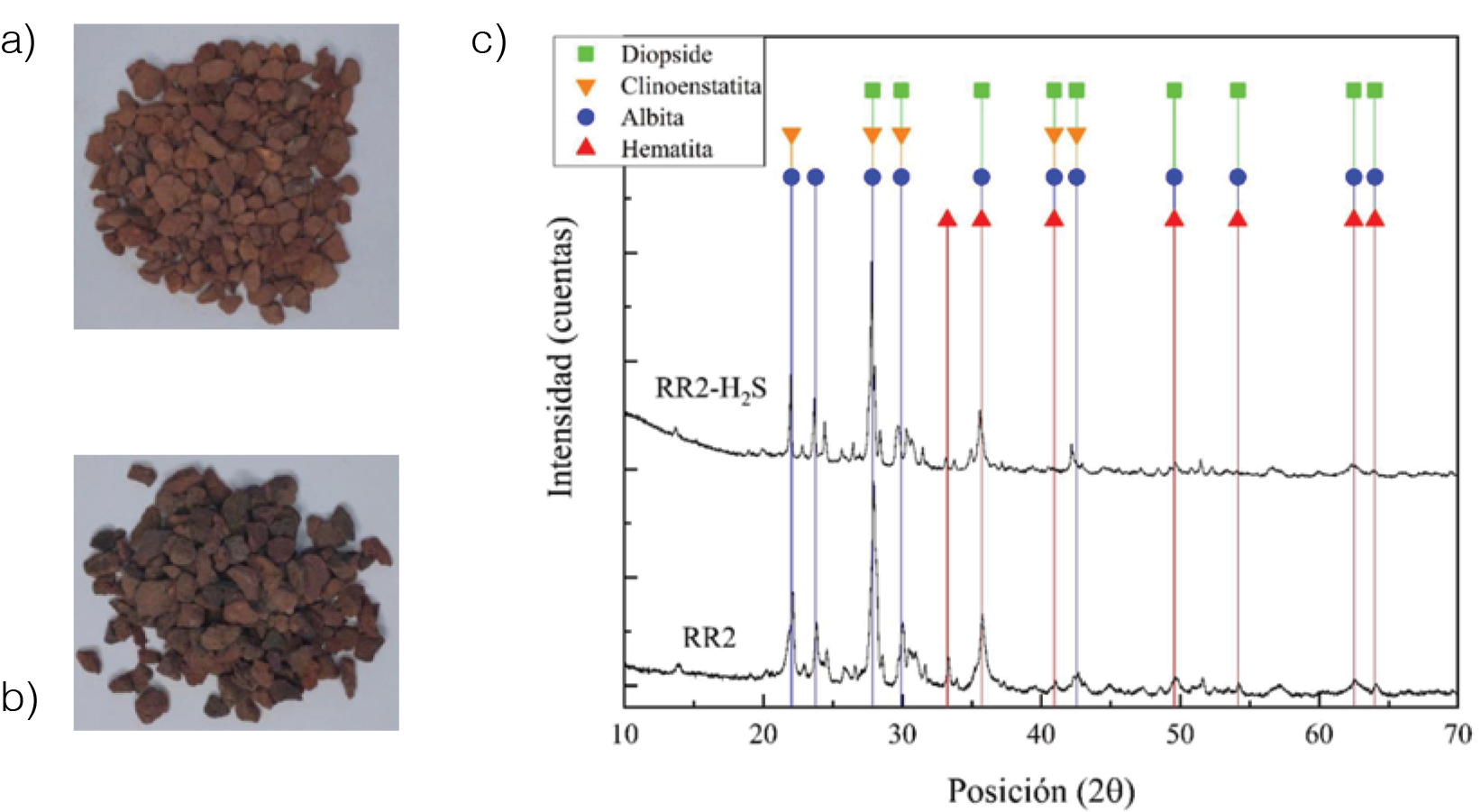
Figura 5. (a) Roca roja original (RR2-P) utilizada como material filtrante. (b) Roca roja reaccionada (RR2-H2S). (c) Difractograma para las rocas roja original (RR2) y reaccionada (RR2-H2S).
La morfología de la superficie de la RR original (RR2) y utilizada (RR2-H2S) se muestran en la Figura 6, donde RR2 muestra algunas porosidades y rugosidades, mientras que la superficie de RR2-H2S es posible notar el colapso de los poros que se atribuyen a la unión del H2S a los sitios activos del material filtrante [9]. La composición elemental de la superficie de los materiales antes y después del paso del biogás a través del medio filtrante obtenidas por EDS, mostradas en la Figura 6(g,h) evidencian la presencia de los elementos O, Si, Al, Na, Ca y Fe, que conforman cada una de las fases minerales identificadas mediante la técnica de XRD y el C del soporte. Después del proceso de desulfuración se detectó la presencia de azufre, que confirma que las RR tienen la capacidad de remover el H2S presente en el biogás y que dicho proceso se lleva a cabo en la superficie del material filtrante [8], [16].
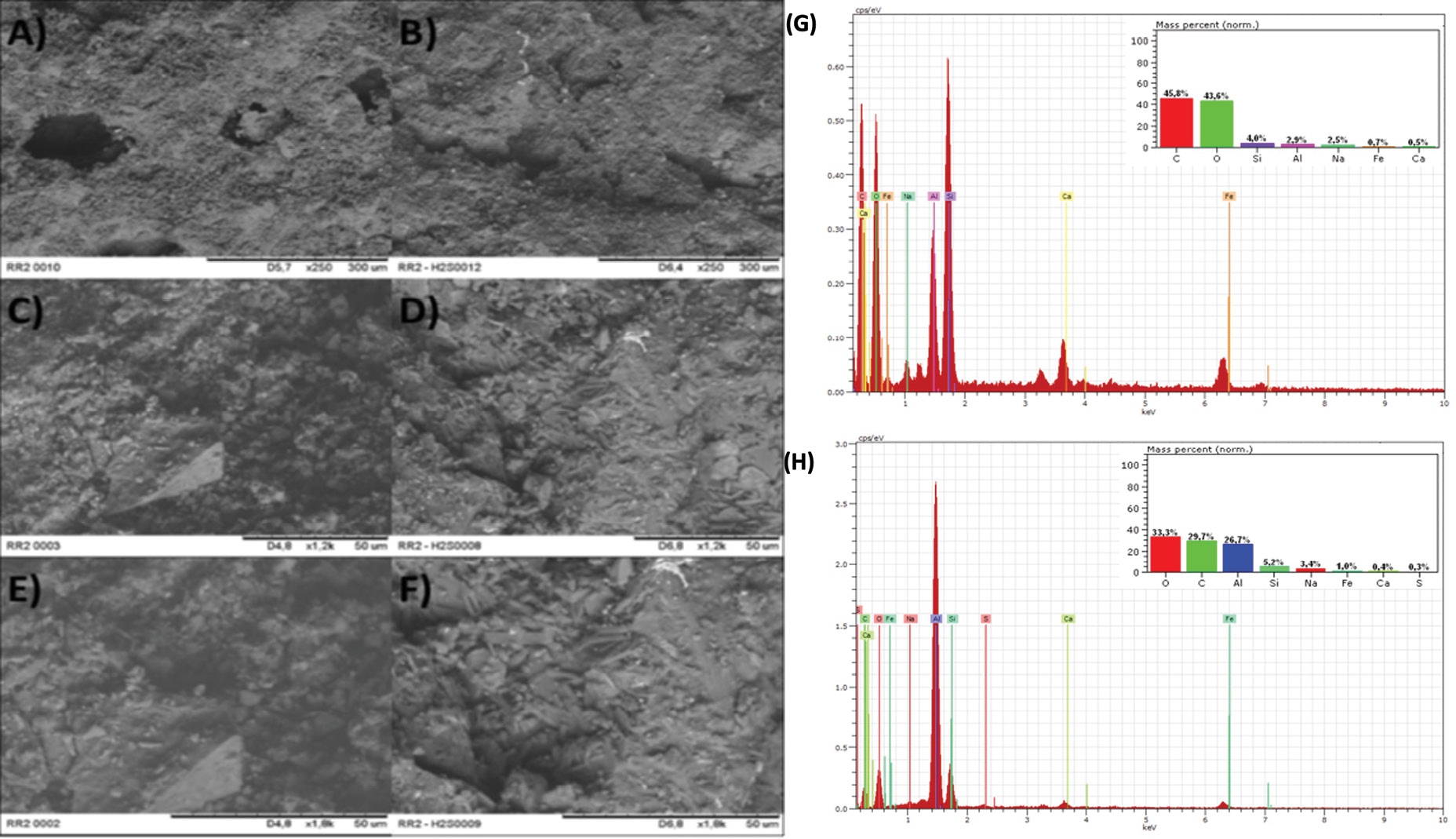
Figura 6 Micrografías SEM para la muestra RR2 antes y después de ser expuestas al biogás. A), C) y E) antes de la exposición al biogás. B), D) y F) después de la exposición al biogás. Magnificación: A) y B) 250x, C) y D) 1.2kx, E) y F) 1.8kx. EDS de RR2 antes y después de ser expuesta a biogás por 30 días
En el cuadro 3, se muestra un resumen comparativo de los resultados obtenidos. La muestra RR2-G presentó una eficiencia de remoción de 23% antes de la reducción en el tamaño de partícula, a pesar de que tenía un contenido inicial de Fe2O3 de 4.8% menor que el indicado para RR3. Esto sugiere que el porcentaje de óxidos de hierro libres en las RR no es proporcional a la cantidad total de hematita presente en los materiales utilizados, sino que otros mecanismos inciden de forma más significativa en su desempeño para absorción de H2S. Mediante la aplicación del ensayo detallado en la norma ASTM designación C97/CM97-09 fue posible evidenciar que al menos para este material el tamaño de partícula del medio filtrante no influye en la capacidad de absorción de agua, y extrapolar que no influye significativamente en el proceso de remoción de H2S. Al comparar el porcentaje de óxido de hierro presente en el material antes y después del proceso de desulfuración, la diferencia encontrada de 3.9% wt., indica que el proceso de remoción del contaminante en estudio suele llevarse a cabo por el intercambio de iones de azufre y oxigeno como se indicó. Esto se verifica al observar el cambio en el color del material utilizado y la identificación de azufre en la superficie del material por EDS.
Cuadro 3. Comparación del desempeño de los medios filtrantes utilizados.
|
Eficiencia de remoción (%) |
Óxido de hierro inicial (%) |
Óxido de hierro final (%) |
Absorción de agua |
Tamaño de partícula (mm) |
|
|
RR2-G |
23 |
4.8 |
- |
11.11 |
> 6.3 |
|
RR3 |
20 |
7.2 |
- |
- |
> 6.3 |
|
RR2-P |
28 |
4.8 |
1.1 |
11.67 |
2.36 - 6.3 |
Conclusiones
En este artículo se reporta una metodología investigativa para estudiar rocas rojas como sustrato para la remoción de H2S, que implicó la recolección y selección de muestras locales, la determinación de su desempeño como filtro desulfurizador y su caracterización química y morfológica. La metodología desarrollada se puede utilizar para investigar otros materiales, posibilitando el desarrollo de sustratos filtrantes accesibles a nivel nacional. Las rocas rojas estudiadas mostraron una capacidad limitada para remover el H2S presente del biogás a temperatura ambiente. Las rocas rojas con un tamaño de partícula mayor a 6.3 mm, RR2 y RR3 alcanzaron una eficiencia de remoción de H2S de 23% y 20%, respectivamente. Al disminuir el tamaño de partícula de RR2 a un rango entre 2.4 y 6.3 mm se mejoró de un 23% a un 28% la eficiencia de remoción de H2S. El porcentaje de absorción de agua (en peso) calculado según lo indicado en la norma ASTM C97-CM97-09 para la roca grande y la roca pequeña fue de 11.11% y de 11.67% respectivamente, lo que permitió evidenciar que el tamaño de partícula no es un parámetro determinante en la mejora de la capacidad absorbente para este material. El análisis de XRD permitió identificar tanto la presencia de óxidos de hierro en las muestras originales, como de las siguientes fases minerales, diopside, clinoenstatita y albita. La presencia de Fe en las muestras determinada mediante XRF para las muestras fue de 5.95% w/w para RR1, 5.17% w/w para RR2 y de 5.20% w/w para RR3. Mediante el uso de XRD-Rietveld se cuantificó que la hematita Fe2O3 presente en las diferentes muestras de roca roja es de 7.2% w/w para RR1 y RR3 y de 4.8% w/w para RR2, la cual disminuye después de exponer el material al H2S de 4.8% a 1.1%. Esta reducción de hematita fue acompañada de un cambio de coloración de rojizo a negro, indicando la formación de compuestos de azufre durante su exposición al H2S. Mediante SEM se identificaron cambios en la morfología de la superficie del material filtrante después de su exposición al H2S, donde es posible observar un colapso en la estructura al mostrarse una superficie más lisa y la presencia de partículas de mayor tamaño. Además, se determinó la presencia de azufre por medio de EDS, debido a la formación de compuestos de azufre a lo largo de la superficie de la roca, generados como productos del proceso de absorción de azufre. Los resultados ofrecen un primer acercamiento al uso de minerales locales para aplicar en procesos de desulfuración de biogás que permitirían robustecer el sector de la biodigestión anaerobia en Costa Rica.
Agradecimientos
Se agradece al profesor Dr. José Luis León Salazar, María Angelica Badilla Sánchez, Fernando Dittel Meza y funcionarios del Centro de Investigación y Extensión en Materiales (CIEMTEC) del TEC por el apoyo brindado en las diferentes etapas de esta investigación. Al Sr. Walter González, propietario de la Finca Los Tejares por permitirnos utilizar el biodigestor durante la fase experimental del proyecto y al geólogo Juan Pablo Solano Monge por el apoyo brindado en la búsqueda de las arcillas. Así como a los funcionarios del Laboratorio de Difracción de Rayos-X, el Laboratorio Institucional de Microscopía (LIM), al Dr. Ricardo Starbird del Centro de Investigación y de Servicios Químicos y Microbiológicos (CEQIATEC) y el Laboratorio de Espectroscopía Óptica, del Instituto Tecnológico de Costa Rica, y a VICESA por su atención y disposición para realizar ensayos necesarios que llevaron a obtener los resultados de esta investigación.
Referencias
[1] F. A. Vélez Bowen, “Adsorción de metano (CH4) de biogás mediante un filtro relleno de un soporte con carbón activado y piedra pómez molida,” 2019.
[2] T. Al Seadi et al., BIOGAS HANDBOOK. 2008.
[3] FAO, “Guía teórico-práctica sobre el biogás y los biodigestores.” Buenos aires, p. 104, 2019.
[4] B. Morero, E. Gropelli, and E. A. Campanella, “Revisión de las principales tecnologías de purificación de biogás,” Cienc. y Tecnol., vol. 1, no. 10, pp. 187–202, 2010.
[5] A. G. Skerman, S. Heubeck, D. J. Batstone, and S. Tait, “Low-cost filter media for removal of hydrogen sulphide from piggery biogas,” Process Saf. Environ. Prot., vol. 105, pp. 117–126, 2017.
[6] FAO, MINENERGIA, PNUD, and GEF, “Manual de Biogás,” Proyecto CHI/00/G32. p. 120, 2011.
[7] A. Petersson, “14. Biogas cleaning,” in The Biogas Handbook: Science, Production and Applications, Woodhead Publishing Limited, 2013, pp. 329–341.
[8] K. Tzu-Hsing, C. Hsin, L. Hsiao-Ping, and P. Ching-Yu, “Red soil as a regenerable sorbent for high temperature removal of hydrogen sulfide from coal gas,” J. Hazard. Mater., vol. 136, no. 3, pp. 776–783, 2006.
[9] R. Mrosso, R. Machunda, and T. Pogrebnaya, “Removal of Hydrogen Sulfide from Biogas Using a Red Rock,” J. Energy, vol. 2020, pp. 1–10, 2020.
[10] M. Garfí, J. Martí-Herrero, A. Garwood, and I. Ferrer, “Household anaerobic digesters for biogas production in Latin America: A review,” Renew. Sustain. Energy Rev., vol. 60, pp. 599–614, 2016.
[11] A.-A. S. M. Magomnang and P. E. P. Villanueva, “Removal of Hydrogen Sulfide from Biogas using Dry Desulfurization Systems,” in International Conference on Agricultural, Environmental and Biological Sciences, 2014, vol. 24–25, pp. 65–68.
[12] L. J. Cihacek and J. M. Bremner, “Characterization of the Sulfur Retained by Soils Exposed to Hydrogen Sulfide,” Commun. Soil Sci. Plant Anal., vol. 24, no. 1–2, pp. 85–92, 1993.
[13] X. M. Meng, W. De Jong, and A. H. M. Verkooijen, “Effect of Hydrothermal Carbonization Reaction Parameters on,” Environ. Prog. Sustain. Energy, vol. 28, no. 3, pp. 360–371, 2009.
[14] A. Davydov, K. T. Chuang, and A. R. Sanger, “Mechanism of H2S oxidation by ferric oxide and hydroxide surfaces,” J. Phys. Chem. B, vol. 102, no. 24, pp. 4745–4752, 1998.
[15] Y. Cao et al., “Low-Temperature H2S Removal from Gas Streams over γ-FeOOH, γ-Fe2O3, and α-Fe2O3: Effects of the Hydroxyl Group, Defect, and Specific Surface Area,” Ind. Eng. Chem. Res., vol. 58, no. 42, pp. 19353–19360, 2019.
[16] R. C. Sahu, R. Patel, and B. C. Ray, “Removal of hydrogen sulfide using red mud at ambient conditions,” Fuel Process. Technol., vol. 92, no. 8, pp. 1587–1592, 2011.
[17] G. E. Alvarado, G. Cárdenes, F. Alvarado, J. Murillo, and M. Arias, “Utilización de rocas ornamentales en Costa Rica desde tiempos precolombinos hasta el siglo XX,” Rev. Geológica América Cent., no. 26, pp. 39–51, 2011.
[18] T. H. Ko and H. Chu, “Spectroscopic study on sorption of hydrogen sulfide by means of red soil,” Spectrochim. Acta - Part A Mol. Biomol. Spectrosc., vol. 61, no. 9, pp. 2253–2259, 2005.
[19] K. Tzu-Hsing, C. Hsin, and T. Jeou-Jen, “Feasibility study on high-temperature sorption of hydrogen sulfide by natural soils,” Chemosphere, vol. 64, no. 6, pp. 881–891, 2006.
[20] B. H. Toby and R. B. Von Dreele, “Appl. Cryst.” pp. 544–549, 2013.
[21] ASTM International, Standard Specification for Woven Wire Test Sieve Cloth and Test Sieves. 2021, pp. 1–9.
[22] ASTM International, “Standard Test Methods for Absorption and Bulk Specific Gravity of Dimension Stone,” ASTM International. pp. 9–11, 2021.
[23] P. Mora Rojas, M. Chaves Flores, M. F. Ellis Chaves, and A. Bejarano Carrillo, “Uso de Biodigestores para el tratamiento de residuos en cercanías del Aeropuerto Juan Santamaría de Costa Rica como instrumento para el control de aves carroñeras,” RedBioLAC, vol. 4, pp. 9–13, 2020.
[24] O. Acevedo-Sandoval, E. Ortiz-Hernández, M. Cruz-Sánchez, and E. Cruz-Chávez, “El papel de óxidos de hierro en suelos,” Terra Latinoaméricana, vol. 22, no. 4, pp. 485–497, 2004.
1 Escuela de Ciencia e Ingeniería de Materiales, Instituto Tecnológico de Costa Rica. Costa Rica. Correo electrónico: fioullsolano@gmail.com
https://orcid.org/0000-0002-0686-5756
2 Biomatech Engineering Ltda, San José. Costa Rica. Correo electrónico: marco.chaves@biomatec.net
https://orcid.org/0000-0001-5995-2979
3 Biomatech Engineering Ltda, San José, San Pedro. Costa Rica. Correo electrónico: luis.urvina@biomatec.net
4 Escuela de Ciencia e Ingeniería de Materiales, Instituto Tecnológico de Costa Rica. Costa Rica. Correo electrónico: cchaves@itcr.ac.cr
https://orcid.org/0000-0002-9924-1562