Evaluación del riesgo químico mediante la aplicación de un índice de seguridad inherente: un caso de estudio en cursos de docencia de química general en un centro universitario
Chemical risk assessment by applying an inherent safety index: a case study in general chemistry teaching courses at a university center
Jose Carlos Mora-Barrantes1, Juan Manuel Sotomayor-Pineda2, Christopher Afú-Méndez3, Jocelyn López-Martínez4, María Alejandra Vallejo-Salas5
Fecha de recepción: 17 de setiembre de 2020
Fecha de aprobación: 18 de enero de 2021
Mora-Barrantes, J.C; Sotomayor-Pineda, J.M; Afú-Méndez, C; López-Martínez, J; Vallejo-Salas, M.A. Evaluación del riesgo químico mediante la aplicación de un índice de seguridad inherente: un caso de estudio en cursos de docencia de química general en un centro universitario. Tecnología en Marcha. Vol. 35-1. Enero-Marzo 2022. Pág 100-114. https://doi.org/10.18845/tm.v35i1.5288
https://doi.org/10.18845/tm.v35i1.5288
Palabras clave
Índice; seguridad inherente; peligro; riesgo; laboratorio; universidad; producto químico.
La Seguridad Inherente (SI) ha tomado una gran importancia durante los últimos años, permitiendo evaluar los riesgos químicos para eliminar o evitar los peligros asociados a procesos químico-físicos, mediante la implementación de protecciones adicionales en las distintas corrientes industriales y a escalas menores como lo son los laboratorios químicos de centros universitarios. El presente trabajo de investigación tiene como objetivo general definir el nivel de riesgo químico presente en curso e Química General desarrolladlos en centros universitarios, mediante la aplicación de un índice de riesgo de seguridad inherente. Durante el trabajo de campo se evaluaron los riesgos de las sustancias químicas y las prácticas experimentales Se recopilo información referente a propiedades fisicoquímicas y tóxicas de las sustancias , para su posterior interpretación de acuerdo las variables utilizadas por el método. Se obtuvo un Índice de seguridad inherente al producto químico (ICI) para cada experimento. En total se evaluaron 123 reactivos químicos de 20 procedimientos experimentales, obteniendo el valor ICI más elevado (١٥) para las prácticas “Reacciones químicas: ecuaciones químicas” y “Valoraciones ácido-base”. En general el nivel de riesgo según los valores experimental obtenidos de ICI para los laboratorios evaluados se consideran bajos, con valores en un rango de entre 2 y 15, en comparación con el valor teórico máximo (23) permitido por la metodología utilizada.
Keywords
Index; inherent safety; hazard; risk; university; laboratory; chemical.
Abstract
The Inherent Safety (IS) has taken on great importance in recent years, allowing chemical risks to be assessed in order to eliminate or avoid hazards associated with physicochemical processes, by implementing additional protection in the various industrial streams as well as on smaller scale production process, like the chemical laboratories of university centers. The main objective of this research is to define the level of chemical risk present in General Chemistry experimental practices developed at university centers, by applying an inherent safety risk index. The risks of the chemicals were evaluated by obtaining physicochemical and toxic properties of the substances and their corresponding comparison with the sub-indices of the evaluation method of the inherent safety index, to finally obtain the Inherent Safety Index of the chemical (ICI) for each experiment. A total of 123 chemical reagents from 20 experimental procedures were evaluated, obtaining the highest ICI value (15) for the practices “Chemical reactions: chemical equations” and “Acid-base titrations”. In general, the level of risk according to the experimental values obtained from ICI for the evaluated laboratories are considered low, with values in a range between 2 and 15, compared to the maximum theoretical value (23) allowed by the methodology used.
Introducción
En los últimos años, el campo de la prevención de pérdidas y la gestión de riesgos ha presentado gran interés en el ámbito académico [1]. Durante el proceso de aprendizaje es común que estudiantes, profesores y personal administrativo del laboratorio estén en contacto continuo con sustancias químicas, por lo que es prescindible salvaguardar la seguridad y la salud de las personas que se exponen a los productos químicos [2]. La medida de seguridad más distinguida, es el riesgo, el cual se define como la probabilidad de una pérdida; que implica dos parámetros mensurables: consecuencia y probabilidad, existen eventos que son más probables de ocurrencia que otros, sin embargo, una consecuencia única de la secuencia de eventos no es posible predecir [3]. En procesos químicos el riesgo está asociado a consecuencias sobre la salud de las personas, daño al medio ambiente y destrucción de instalaciones, causados por factores técnicos, errores humanos y factores de gestión y organización [4].
Los efectos causados por sustancias químicas sobre la salud se catalogan como riesgos potenciales agudos, los que pueden provocar irritación y sensibilización aguda entre algunas de sus consecuencias, mientras los riesgos crónicos pueden ocasionar considerables problemas respiratorios dado a su constante exposición [5] [6] [7]. Por otra parte, liberaciones accidentales de emisiones, vertidos y fugas de productos químicos al ambiente son los principales generadores de problemas ambientales de toxicidad, calentamiento global, deposición de ácido y agotamiento de la capa de ozono [8].
En los laboratorios de experimentación de centros de enseñanza superior existen variables de riesgos químicos, debido al almacenamiento de diferentes sustancias con características fisicoquímicas como ser inflamables, explosivos y tóxicos. Además, las instalaciones de los laboratorios disponen de dispositivos eléctricos que comúnmente se encuentran en estado de alta temperatura y presión, provocando vulnerabilidad al fuego y explosiones, por lo que es necesario su correcta caracterización y determinación de los peligros intrínsecos [9] [10].
La evaluación del riesgo químico es indispensable para una adecuada identificación de los peligros químicos asociados a las diferentes sustancias químicas a las que se exponen los usuarios. La evaluación evita y reduce el riesgo durante todo el ciclo de vida del lugar de trabajo [11]the suggested risk reduction alternatives merely focus on added passive and active safety systems rather than preventing or minimising the inherent hazards at source through application of inherently safer design (ISD. Producto de los peligros y riesgos químicos presentes en las diferentes corrientes industriales y a escalas menores (laboratorios químicos), han surgido variadas metodologías para la evaluación del riesgo [1] [3].
Entre algunas metodologías está la relacionada con la seguridad inherente (SI) de los procesos, la cual considera las propiedades intrínsecas del proceso a evaluar. La seguridad inherente es una técnica cuyo principal objetivo es eliminar o evitar los peligros, en lugar de limitarlos mediante la implementación de protecciones adicionales [1][3]. Los principios de la SI se fundamentan en la minimización y sustitución de recursos, y en la atenuación y simplificación de los procesos, lo cual permite seleccionar rutas de procesos químicos inherentes más ecológicas, saludables y seguras [12] [13].
Durante la evaluación de la seguridad inherente en determinado proceso químico se debe considerar la fiabilidad y la confiabilidad del sistema, estos se definen como las probabilidades de que el sistema trabaje correctamente en condiciones extremas y adecuadas respectivamente [14]. Para asegurar un correcto funcionamiento de la aplicación del método de evaluación del riesgo químico mediante el uso de la seguridad inherente es necesario examinar propiedades propias del proceso como: la identificación de las interacciones químicas de las sustancias, el adecuado control del inventario de sustancias químicas, temperaturas y presiones de trabajo, la disposición y adquisición de equipos de seguridad y la infraestructura física del proceso [3].
La evaluación del riesgo mediante la SI implica además el conocimiento de las propiedades fisicoquímicas y toxicológicas de las sustancias utilizadas en los distintos procesos químicos y/o procedimientos analíticos. Otro aspecto por considerar es la capacidad de absorción de una sustancia en el organismo [3].
Otros aspectos específicos del producto químico utilizado que se deben evaluar son: la inflamabilidad de gases y vapores de líquidos inflamables, el riesgo de ignición del químico que puede provocar un incendio o una explosión, la corrosividad de la sustancia con que se trabaja la cual reduce la fiabilidad y la integridad del lugar de trabajo, y la cantidad de calor generado en los procesos [3].
El presente trabajo de investigación tiene como objetivo definir el nivel de riesgo químico presente en cursos de Química General desarrollados en centros universitarios, mediante la aplicación de un índice de riesgo de seguridad inherente, para la prevención de los riesgos hacia la salud de las personas y el medio ambiente, así como para una adecuada escogencia de prácticas de laboratorio que consideren criterios de salud, seguridad y ambiente.
Metodología
La clasificación de las sustancias químicas según sus peligros y riesgos intrínsecos se realizó para las practicas experimentales de los cursos de química general I y II de la Universidad Nacional de Costa Rica. Se utilizó el manual de laboratorio “Química Experimental: Un enfoque hacia la Química Verde” [15]. El manual consta de 25 experimentos en los que se ilustra de forma práctica los conceptos básicos más relevantes sobre los cuales se fundamenta la química. Cada sesión de laboratorio comprende 3 horas semanales de trabajo, durante el cual los estudiantes y funcionarios manipulan y se exponen a sustancias químicas con potenciales riesgos a la salud.
Para determinar el nivel de riesgo químico de los reactivos químicos y experimentos realizados, se aplicó un método de evaluación denominado “índice de seguridad inherente”. Para cada uno de los reactivos químicos se recopiló datos relacionados con su interacción química, inflamabilidad, explosividad, exposición tóxica, corrosividad y el cambio en la entalpía de reacción involucrada. La información tabulada permitió obtener los valores de los diferentes subíndices utilizados por el método de seguridad inherente.
La fuente principal de información para la recopilación de las propiedades fisicoquímicas y toxicológicas, así como las variables del índice de seguridad inherente fueron las MSDS de cada producto y fichas de seguridad de los reactivos en bases de datos de Carl Roth, Labchem y Reactivos Meyer [16] [17] [18].
Para obtener el índice de seguridad inherente (ICI) de cada uno de los experimentos realizados en las prácticas de laboratorio se utilizó como material de apoyo bibliográfico la metodología implementada por Heikkilä [3]. El índice total se obtiene a partir de los siguientes subíndices propuestos por Heikkilä: subíndice de calor de reacción (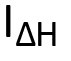 ), subíndice de interacción química (IINT), subíndice de inflamabilidad (IFL), subíndice de exposición tóxica (ITOX), subíndice de explosividad (IEX) y subíndice de corrosividad (ICOR).
), subíndice de interacción química (IINT), subíndice de inflamabilidad (IFL), subíndice de exposición tóxica (ITOX), subíndice de explosividad (IEX) y subíndice de corrosividad (ICOR).
El subíndice 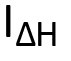 del calor de reacción se utilizó el cambio de entalpia de reacción (ΔHR J/g) de cada producto químico, primero se obtuvo la entalpía de formación (ΔHf J/g) de cada reactivo a partir del libro “Handbook of Chemistry and Physics” [19] y del archivo de “Datos Termodinámicos” de Borgogno [20], posteriormente se aplicó la siguiente ecuación para obtener las entalpías de reacción:
del calor de reacción se utilizó el cambio de entalpia de reacción (ΔHR J/g) de cada producto químico, primero se obtuvo la entalpía de formación (ΔHf J/g) de cada reactivo a partir del libro “Handbook of Chemistry and Physics” [19] y del archivo de “Datos Termodinámicos” de Borgogno [20], posteriormente se aplicó la siguiente ecuación para obtener las entalpías de reacción:

Se compararon los valores obtenidos por las entalpías de reacción con los valores presentes en el cuadro 1 para obtener el subíndice 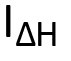 .
.
Cuadro 1. Determinación de los subíndices del calor de reacción.
|
Calor de reacción / masa de reacción total |
Puntuación |
|
Térmicamente neutro ≤ 200 J/g |
0 |
|
Ligeramente exotérmico <600 J/g |
1 |
|
Moderadamente exotérmico <1200 J/g |
2 |
|
Fuertemente exotérmico <3000 J/g |
3 |
|
Extremadamente exotérmico ≥ 3000 J/g |
4 |
Fuente: A. Heikkilä, 1999.
El subíndice de interacción química se obtuvo de los datos del cuadro 2, la información de cada producto químico ( Sección 10 -estabilidad y reactividad de las sustancias) de la MSDS y el uso de las indicaciones de peligro (frases H) del Sistema Globalmente Armonizado (SGA).
Cuadro 2. Determinación del subíndice IINT de interacción química.
|
Interacción química |
Puntuación del IINT |
|
Formación de calor |
1 – 3 |
|
Fuego |
4 |
|
Formación de gas inofensivo, no inflamable |
1 |
|
Formación de gases tóxicos |
2 – 3 |
|
Formación de gases inflamables |
2 – 3 |
|
Explosión |
4 |
|
Polimerización rápida |
2 – 3 |
|
Químicos tóxicos solubles |
1 |
Fuente: A. Heikkilä, 1999.
La definición del subíndice de inflamabilidad de cada producto químico, se obtuvo los valores de punto de inflamación y posteriormente se compararon con el siguiente cuadro.
Cuadro 3. Determinación del subíndice de inflamabilidad IFL.
|
Inflamabilidad |
Puntuación del IFL. |
|
0 |
|
|
Combustible (punto de inflamación > 55°C) |
1 |
|
Inflamable (punto de inflamación ≤ 55°C) |
2 |
|
Fácilmente inflamable (punto de inflamación < 21°C) |
3 |
|
Muy inflamable (punto de inflamación < 0°C y punto de ebullición ≤ 35°C) |
4 |
Fuente: A. Heikkilä, 1999.
La determinación del subíndice de exposición tóxica de cada producto químico, se utilizaron los valores de TLV obtenidos de las MSDS, y se compararon con los criterios y valores obtenidos a partir del cuadro 4.
Cuadro 4. Determinación del subíndice ITOX de exposición tóxica.
|
Límite tóxico (ppm) |
Puntuación de ITOX |
|
0 |
|
|
TLV ≤ 10000 |
1 |
|
TLV ≤ 1000 |
2 |
|
TLV ≤ 100 |
3 |
|
TLV ≤ 10 |
4 |
|
TLV ≤ 1 |
5 |
|
TLV ≤ 0.1 |
6 |
Fuente: A. Heikkilä, 1999.
Los criterios para definir el valor del subíndice de explosividad se obtuvieron a partir del rango de explosividad (UEL-LEL) de cada sustancia y se compararon con los datos mostrados en el siguiente cuadro.
Cuadro 5. Determinación del Subíndice IEX de Explosividad.
|
Explosividad (UEL-LEL) vol % |
Puntuación de IEX |
|
No explosivo |
0 |
|
0 – 20 |
1 |
|
20 – 45 |
2 |
|
45 – 70 |
3 |
|
70 – 100 |
4 |
Fuente: A. Heikkilä, 1999.
El subíndice de corrosividad consideró el material del recipiente en que se almacena el reactivo químico, reactivos químicos almacenados en vidrio se les asignó un valor de cero, mientras que en el caso de los almacenados en algún recipiente metálico se les asignó un valor de 1. Recopiladas las variables para cada uno de los reactivos químicos, se determinó el índice de seguridad inherente para cada experimento según la siguiente fórmula:
Se generaron bases de datos y patrones de distribución de los reactivos químicos y experimentos utilizados en las prácticas de docencia de los cursos experimentales de química general I y II. Con la información del índice de seguridad inherente de cada uno de los laboratorios, se calculó un porcentaje de error, restando el valor teórico máximo del índice al valor experimental del índice, multiplicado por cien, entre el valor teórico máximo del índice.
Resultados
En total se evaluaron 20 procedimientos experimentales, de los cuales 8 corresponden al curso de Laboratorio de Química General I (LQGI) [21] y 12 al curso de Laboratorio de Química General II (LQGII) [22]. La cantidad de reactivos evaluados son de 65 y 58 para los cursos de LQGI y LQGII respectivamente, para un total final de 123 reactivos químicos evaluados.
Química General I: el Índice de seguridad inherente al producto químico (ICI)
Para este curso, solo se tomaron en consideración ocho de las trece prácticas que componen el curso, debido a que las restantes cinco no hacen uso de productos químicos o incluso se realizan de manera remota mediante el uso de simuladores. En el cuadro 6 se muestra el nombre de cada practica evaluada, la cantidad de reactivos químicos evaluados por práctica, y la lista de algunos de los reactivos químicos utilizados.
Cuadro 6. Cantidad de productos químicos evaluados en las distintas prácticas realizadas en el curso de Laboratorio de Química General I.
|
Nombre de la práctica |
Siglas de la Práctica |
Cantidad de Sustancias Evaluadas |
Ejemplos de Reactivos Químicos Analizados |
|
Seguridad en el laboratorio |
SL |
8 |
Cloroformo, Hidróxido de Sodio |
|
Uso de la balanza y del equipo de medición de volumen |
BV |
2 |
Ácido acetilsalicílico, cafeína |
|
Relaciones estequiométricas |
RE |
4 |
Carbonato de Sodio, Bicarbonato de sodio |
|
Síntesis de la aspirina |
SA |
5 |
Ácido fosfórico, Ácido acetilsalicílico, Ácido acético |
|
Reacciones químicas: ecuaciones químicas |
RQ |
23 |
Cloruro de hierro (III), Sulfato de sodio, Fosfato de sodio |
|
Identificación de cationes Fe3+, Ca2+ y NH4+ |
IC |
8 |
Carbonato de sodio, Tiocianato de potasio |
|
Entalpía de neutralización y Ley de Hess |
LH |
6 |
Ácido clorhídrico, Hidróxido de amonio |
|
Polaridad molecular y fuerzas intermoleculares |
PM |
9 |
1-butanol, Etanol, 1-pentanol |
|
Total |
- |
65 |
- |
En el cuadro 7 se muestra un ejemplo de los datos recopilados para el experimento “Síntesis de la aspirina”. La información mostrada en el cuadro 7 se generó para las 8 prácticas del curso de química general I según los datos correspondientes para cada experimento.
Cuadro 7. Propiedades fisicoquímicas de las sustancias utilizadas en el experimento “Síntesis de la aspirina” para obtener los subíndices de seguridad inherente al producto químico.
|
Sustancia Química |
ΔH reacción (J/g) |
Interacción química |
P. Inflamabilidad (°C) |
Rango Inflamabilidad/ Explosividad (%) |
TLV (ppm) |
Material de almacenamiento |
|
Ácido salicílico |
-507.01 |
H302, H318, H361d |
157 |
1.1% a 200°C |
0,69 |
Vidrio |
|
Anhidro acético |
-507.01 |
H226, H302+H332, H314 |
49 |
2 - 10% |
5 |
Vidrio |
|
Ácido fosfórico |
0 |
H290, H314 |
NA |
NA |
0.25 |
Vidrio |
|
Ácido acetilsalicílico |
-507.01 |
NA |
NA |
NA |
0.68 |
Vidrio |
|
Ácido acético |
-507.01 |
H314, H318, |
39 |
4 - 17 % |
10 |
Vidrio |
Con la información mostrada en el cuadro 7 se obtuvo el valor de los diferentes subíndices que conforma el ICI, estos son; IΔH, IINT, IFL, IEX, ITOX e ICOR. Los valores de estos subíndices para los reactivos químicos incluidos en el cuadro 7 se muestran en el cuadro 8. El valor ICI para el experimento de Síntesis de la aspirina” es 12. De igual forma se obtuvieron los valores de los subíndices y del ICI para el resto de las 8 prácticas que conforman el curso.
Cuadro 8. Índice de seguridad inherente al producto químico a partir de los respectivos subíndices de las sustancias químicas evaluadas en la práctica “Síntesis de la aspirina”.
|
Sustancia Química |
IΔH |
IINT |
IFL |
ITOX |
IEX |
ICOR |
ICI |
|
Ácido salicílico |
1 |
1 |
1 |
0 |
1 |
0 |
12 |
|
Anhidro acético |
1 |
3 |
2 |
4 |
1 |
0 |
|
|
Ácido fosfórico |
0 |
1 |
0 |
5 |
0 |
0 |
|
|
Ácido acetilsalicílico |
1 |
1 |
0 |
5 |
0 |
0 |
|
|
Ácido acético |
1 |
4 |
2 |
4 |
1 |
0 |
El cuadro 9 muestra los valores individuales de los subíndices, así como el valor final del Índice de seguridad inherente al producto químico (ICI) para cada práctica.
Cuadro 9. Índices de seguridad inherente al producto químico (ICI) del laboratorio de Química General. I
|
Inicial de la práctica |
IΔH,max |
IINT,max |
IFL,max |
ITOX,max |
IEX,max |
ICOR,max |
ICI,Exp |
|
SL |
0 |
4 |
2 |
4 |
1 |
0 |
11 |
|
BV |
0 |
1 |
0 |
5 |
0 |
0 |
6 |
|
RE |
0 |
4 |
0 |
5 |
0 |
0 |
9 |
|
SA |
1 |
4 |
2 |
4 |
1 |
0 |
12 |
|
RQ |
4 |
4 |
3 |
0 |
4 |
0 |
15 |
|
IC |
0 |
3 |
0 |
5 |
0 |
0 |
8 |
|
LH |
1 |
4 |
2 |
4 |
1 |
0 |
12 |
|
PM |
0 |
3 |
4 |
2 |
1 |
0 |
10 |
|
Total |
6 |
27 |
13 |
29 |
8 |
0 |
83 |
Con respecto al valor de ICI, el menor valor obtenido es de 6 mientras que el máximo valor reportado es de 15. Los menores valores corresponden a las prácticas de BV (6), RE (9) y IC (8), esto obedece principalmente a que estas prácticas no presentan ninguna reacción química durante la duración de la práctica; para esas 3 prácticas el ITOX,max es el componente que realiza el mayor aporte al cálculo del ICI. Por su parte el mayor valor (15) corresponde al experimento denominado RQ, que se debe principalmente a que la variable o subíndice que mayor aporta a este valor es IΔH,max , que obtuvo el valor máximo(4) que permite el método; debido a que la principal reacción química presenta un valor de entalpia muy exotérmico. Otras prácticas con valores importantes son las de SA y LH, con un valor de ICI de 12 cada uno. Estos valores obedecen fundamentalmente al valor de IINT,max obtenido por estas prácticas(4), además que el valor de la sumatoria de los índices IFL,max, ITOX,max e IEX,max, contemplo el máximo valor experimental (7). La práctica SA utiliza reactivos químicos con el anhidro acético y la práctica LH ácido acético, los cuales presentan propiedades de ser sustancias tóxicas, inflamables y explosivas .-
Según el cuadro anterior el menor valor obtenido para el IΔH,max es de 0, mientras que el máximo valor reportado es de 4. Los menores valores corresponden a las prácticas de SL, BV, RE, IC y PM; esto obedece principalmente a que estas prácticas no presentan reacciones químicas relevantes durante su procedimiento. Por su parte el mayor valor (4) corresponde al experimento denominado RQ, lo que se debe principalmente a que esta práctica presenta una reacción química cuyo valor de entalpia resulta muy exotérmico, alrededor de –18754,31 J/g. Respecto al IINT,max se obtuvo que la mayoría de los procedimientos, presentaron el valor máximo (4). Esto obedece a que se trabaja con reactivos que presentan características de ser explosivas e inflamables. Para la determinación del IFL,max, se obtuvo que la práctica PM presenta el mayor valor (4), debido a la presencia de hexano durante su sesión de trabajo, que es el reactivo con menor punto de inflamabilidad de los analizados. Con relación al ITOX,max, se encontró que la práctica RQ posee el menor valor (0), mientras que las prácticas BV, RE e IC presentan las tres el mayor valor (5); esto debido a que los rangos de TLV-TWA fueron bastante amplios, con un valor máximo de 5000 ppm para el CO2 y un valor mínimo de 0,01 ppm para el sulfato de cobre (II) pentahidratado (CuSO4*5H2O). La práctica RQ presento el mayor valor de IEX,max (4), debido a que se da la formación de hidrógeno como producto de la reacción química principal, este compuesto presenta un rango de explosividad muy amplio (límite inferior= 4 % y límite superior= 75 %), por lo que el método le otorga el valor (4) máximo para este rubro. Por último, para el ICOR,max todas las prácticas obtuvieron la puntuación mínima de 0, indicativo de que se utilizan sustancias poco corrosivas, las cuales se almacenan en recipientes de vidrio y plástico.
En el cuadro 9 se observa que los valores ICI no varían bruscamente de un experimento a otro, manteniéndose en un rango de entre 6-15. De acuerdo con el método utilizado el máximo valor teórico de Índice de seguridad inherente que una práctica o proceso químico puede obtener es de 23.
Se graficaron los valores de ICI de cada una de las diferentes prácticas analizadas contra el máximo valor que permite el método, los resultados se muestran en el gráfico 1. Por lo tanto, los datos obtenidos experimentalmente indican que las prácticas no poseen una peligrosidad alta, debido a que como se aprecia en el gráfico 1. Todas las prácticas poseen una diferencia considerable respecto al máximo valor permitido. La práctica con valor experimental más cercano al valor teórico corresponde a RQ con un valor de 15 y la que presenta un valor menos cercano es BV con un valor de 6.
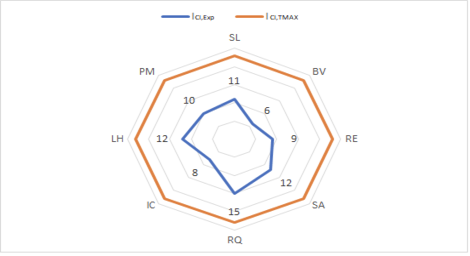
Figura 1. Comparación de los Índices de seguridad inherente al producto químico (ICI) de las prácticas del Laboratorio de Química General I, respecto al máximo valor teórico de 23.
La información de la figura 1 se complementa con los porcentajes de erros incluidos en el cuadro 10 para las prácticas BV y RQ, consideradas la más segura y la más peligrosa respectivamente. A menor porcentaje de error mayor el nivel de riesgo de la práctica. Esos valores se obtienen debido a que el porcentaje de error depende de la diferencia que existe entre el valor de ICI,Exp y el ICI,TMAX y permiten demostrar de una forma cuantitativa lo ilustrado en el gráfico 1. Para el resto de las practicas los porcentajes de error están en un rango de entre 47,83 % y 73,91 %.
Cuadro 10. Porcentaje de error de los Índices de seguridad inherente al producto químico (ICI) de las prácticas “Uso de la balanza y del equipo de medición de volumen” y “Reacciones químicas: ecuaciones químicas”.
|
Inicial de la Práctica |
ICI,Exp |
ICI,TMAX |
% Error |
|
BV |
6 |
23 |
73,91 |
|
RQ |
15 |
23 |
34,78 |
Química General II: el Índice de seguridad inherente al producto químico (ICI)
Para este curso en particular se estudiaron las doce prácticas. En el cuadro 11 se muestra el nombre de cada práctica evaluada, la cantidad de reactivos químicos evaluados por práctica y la lista de algunos de los reactivos químicos utilizados.
Cuadro 11. Cantidad de productos químicos evaluados en las distintas prácticas realizadas en el curso de Laboratorio de Química General II.
|
Nombre de la práctica |
Inicial de la Práctica |
Cantidad de Sustancias Evaluadas |
Ejemplos de Reactivos Químicos Analizados |
|
Calor de fusión del agua |
CA |
1 |
Agua |
|
Propiedades de los líquidos |
PL |
3 |
Acetona gas, Acetona líquida, Glicerina |
|
Disoluciones, preparaciones y caracterizaciones |
DS |
7 |
Ácido benzoico, Bicarbonato de sodio |
|
Propiedades coligativas |
PC |
2 |
Cloruro de sodio, Sulfato de cobre |
|
Cinética de una reacción |
CR |
2 |
Ácido sulfámico, Nitrito de sodio |
|
Principio de Le Chatelier |
LC |
6 |
Ácido clorhídrico, Cloruro de aluminio |
|
Sustancias ácidas, básicas e indicadores de pH |
AB |
17 |
Ácido acético, Acetato de sodio, Cloruro de sodio |
|
Valoraciones ácido-base |
VL |
4 |
Ácido ascórbico, Ácido acético, Ftalato ácido de potasio |
|
Disolución Amortiguadora |
DA |
4 |
Fosfato ácido de potasio, Fosfato diácido de potasio, |
|
Determinación de Kps |
DK |
4 |
Ácido clorhídrico, Hidróxido de calcio |
|
Segunda Ley de la Termodinámica |
ST |
3 |
Bicarbonato de sodio, Hidróxido de calcio |
|
Electroquímica: celdas y electrodeposición |
EQ |
5 |
Cloruro de potasio, Fenolftaleína, Sulfato de cobre (III) |
|
Total |
- |
58 |
- |
En el cuadro 12 se muestra un ejemplo de los datos recopilados para el experimento “Determinación de Kps”. La información mostrada en el cuadro 12 se generó para las doce prácticas del curso de química general II.
Cuadro 12. Propiedades fisicoquímicas de las sustancias utilizadas en el experimento “Determinación de Kps” para obtener los subíndices de seguridad inherente al producto químico.
|
Sustancia Química |
ΔH reacción (J/g) |
Interacción química |
P. Inflamabilidad (°C) |
Rango Inflamabilidad/ Explosividad (%) |
TLV (ppm) |
Material de almacenamiento |
|
Hidróxido de calcio |
-16895,24 |
H290 Corrosivo para metales |
NA |
NA |
NA |
Vidrio |
|
Ácido clorhídrico |
-16895,24 |
H290 Corrosivo para metales |
NA |
NA |
5 |
Vidrio |
|
Hidróxido de magnesio |
-14812,60 |
NA |
NA |
NA |
NA |
Vidrio |
|
Púrpura de bromocresol |
0 |
NA |
NA |
NA |
NA |
Vidrio |
Con la información mostrada en el cuadro 12 se obtuvo el valor de los diferentes subíndices que conforma el ICI, estos son; IΔH, IINT, IFL, IEX, ITOX e ICOR. Los valores de estos subíndices para los reactivos químicos incluidos en el cuadro 12 se muestran en el siguiente cuadro. El valor ICI para la práctica “determinación de Kps” es de 11. De igual forma se obtuvieron los valores de los subíndices y del ICI para el resto de las once prácticas que conforman el curso.
Cuadro 13. Índice de seguridad inherente al producto químico a partir de los respectivos subíndices de las sustancias químicas evaluadas en la práctica “Determinación de Kps”.
|
Sustancia Química |
IΔH |
IINT |
IFL |
ITOX |
IEX |
ICOR |
ICI |
|
Hidróxido de calcio |
4 |
1 |
0 |
4 |
0 |
0 |
11 |
|
Ácido clorhídrico |
4 |
3 |
0 |
4 |
0 |
0 |
|
|
Hidróxido de magnesio |
4 |
1 |
0 |
0 |
0 |
0 |
|
|
Púrpura de bromocresol |
0 |
1 |
0 |
0 |
0 |
0 |
El cuadro 14 muestra los valores individuales de los subíndices, así como el valor final del Índice de seguridad inherente al producto químico (ICI) para cada práctica.
Cuadro 14. Índices de seguridad inherente al producto químico (ICI) del laboratorio de Química General II a partir de los máximos valores de los subíndices obtenidos en cada práctica.
|
Inicial de la práctica |
IΔH,max |
IINT,max |
IFL,max |
ITOX,max |
IEX,max |
ICOR,max |
ICI,Exp |
|
CA |
1 |
1 |
0 |
0 |
0 |
0 |
2 |
|
PL |
1 |
4 |
4 |
1 |
2 |
0 |
12 |
|
DS |
4 |
4 |
0 |
5 |
0 |
0 |
13 |
|
PC |
0 |
1 |
0 |
5 |
0 |
0 |
6 |
|
CR |
0 |
1 |
0 |
4 |
0 |
0 |
5 |
|
LC |
4 |
4 |
0 |
5 |
0 |
0 |
13 |
|
AB |
0 |
4 |
2 |
4 |
1 |
0 |
11 |
|
VL |
4 |
4 |
2 |
4 |
1 |
0 |
15 |
|
DA |
0 |
3 |
0 |
4 |
0 |
0 |
7 |
|
DK |
4 |
3 |
0 |
4 |
0 |
0 |
11 |
|
ST |
0 |
4 |
0 |
4 |
0 |
0 |
8 |
|
EQ |
3 |
1 |
0 |
5 |
0 |
0 |
9 |
|
Total |
21 |
34 |
8 |
45 |
4 |
0 |
112 |
Con respecto al valor de ICI, el menor valor obtenido es de 2, para la práctica denominada “Calor de fusión del agua”, mientras que el máximo valor reportado es de 15, que corresponde a la práctica denominada “Valoraciones ácido-base”. Otras prácticas con valores menores corresponden a las prácticas de PC (6), CR (5), DA (7) y ST (8), esto obedece principalmente a que estas prácticas no presentan ninguna reacción química dentro de su procedimiento. Para esas cuatro prácticas el ITOX,max el componente que realiza el mayor aporte al cálculo del ICI; una excepción a este comportamiento se visualiza en el procedimiento EQ, que presenta un valor de índice bajo (9), y sin embargo, el valor final de ICI,Exp obedece a la presencia de reacciones exotérmicas, siendo asignado un valor de 3 al subíndice de IΔH,max. Por su parte, el mayor valor de ICI,Exp (15) corresponde al experimento denominado VL, lo cual se debe principalmente al aporte del valor del IΔH,max (4). Otras prácticas con valores importantes son las de DS (13), LC (13) y DK (11). Estos valores son producto de los valores de los subíndices IΔH,max y el IINT,max producto de los reactivos químicos utilizados como carbonato de sodio, cloruro de cobalto (II) y nitrato de potasio.
Según el cuadro 14 el menor valor obtenido para el IΔH,max es de 0, mientras que el máximo valor reportado es de 4. Los menores valores corresponden a las prácticas de PC, CR, AB, DA y ST; esto obedece principalmente a que estas prácticas no presentan reacciones químicas relevantes durante su procedimiento. Por su parte, el mayor valor (4) corresponde a las prácticas denominadas DS, LC, VL y DK, lo que se debe principalmente a que estas prácticas presentan reacciones químicas con valores de entalpías de reacción exotérmicas que oscilan entre -5000 y -17000 J/g. Respecto a el IINT,max se obtuvo que la mayoría de los procedimientos presentaron el valor máximo que indica el método (4),lo cual se debe principalmente al uso de reactivos con características explosivas e inflamables. La práctica PL presentó el mayor valor del IFL,max (4) e IEX,max (2), resultado del uso de de acetona, reactivo con un punto de inflamabilidad altamente bajo(-17 °C) y con propiedades explosivas. Con relación al ITOX,max, se encontró que la práctica CA posee el menor valor (0), mientras que las prácticas DS, PC, LC y EQ presentan el mayor valor (5). Para estas 4 practicas los rangos de TLV-TWA presentan un valor máximo de 250 ppm, que corresponde a la acetona, mientras que el valor mínimo lo posee el indicador de pH conocido como “Rojo Congo” ( TWA = 0,11 ppm).
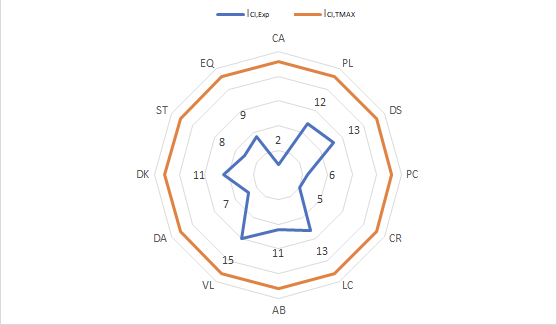
Figura 2. Comparación de los Índices de seguridad inherente al producto químico (ICI) de las prácticas del Laboratorio de Química General II, respecto al valor teórico máximo de 23.
De acuerdo con el método utilizado el máximo valor Índice de seguridad inherente que una práctica o proceso químico puede obtener es de 23. Se graficaron los valores de ICI de cada una de las diferentes prácticas analizadas contra el máximo valor que permite el método, los resultados se muestran en la figura 2. Los datos obtenidos experimentalmente indican que igual a lo observado en el curso de química general I, las prácticas son consideradas con un nivel de resigo seguro, producto de la diferencia de los datos experimentales respecto al máximo valor permitido. De la figura 2 se observa que la práctica VL presenta el mayor nivel de peligro (15),mientras que la práctica CA se cataloga como la más segura al presentar un valor experimental (2) más lejano al teórico.
Cuadro 15. Porcentaje de error de los Índices de seguridad inherente al producto químico (ICI) experimentales de las prácticas Calor de fusión del agua” y “Valoraciones ácido-base”.
|
Inicial de la práctica |
ICI,Exp |
ICI,TMAX |
% Error |
|
CA |
2 |
23 |
91,30 |
|
VL |
15 |
23 |
34,78 |
El cuadro 15 muestra el porcentaje de error para las prácticas CA y VL, consideradas la más segura y la más peligrosa. Los valores son respectivamente. Para el resto de las practicas los porcentajes de error están en un rango de entre 43,48 % y 78,26 %.
Comparación del nivel de riesgo (ICI) - Cursos de química general I y II
El cuadro 16 contiene los ICI,Exp de cada practica y su respectivo ICI,TMAX. . Con base en estos datos se tabularon los valores de porcentaje de error obtenido para cada práctica, así como el % de error experimental promedio de cada curso.
Según el cuadro 16, los valores obtenidos de porcentaje de error para el ICI,Exp no presenta una diferencia significativa, los valores son 54,89% para Química General I y 59,42% para Química General II. Estos resultados nos indican que ambos laboratorios no presentan un nivel de peligrosidad alto.
Cuadro 16. Porcentaje de error de los Índices de seguridad inherente al producto químico (ICI) experimentales de los laboratorios de Química General I y II.
|
Curso |
Inicial de la Práctica |
ICI,Exp |
ICI,TMAX |
% Error |
|
SL |
11 |
23 |
52,17 |
|
|
BV |
6 |
23 |
73,91 |
|
|
RE |
9 |
23 |
60,87 |
|
|
SA |
12 |
23 |
47,83 |
|
|
RQ |
15 |
23 |
34,78 |
|
|
IC |
8 |
23 |
65,22 |
|
|
LH |
12 |
23 |
47,83 |
|
|
PM |
10 |
23 |
56,52 |
|
|
Total |
- |
83 |
184 |
54,89 |
|
Química general II |
CA |
2 |
23 |
91,30 |
|
PL |
12 |
23 |
47,83 |
|
|
DS |
13 |
23 |
43,48 |
|
|
PC |
6 |
23 |
73,91 |
|
|
CR |
5 |
23 |
78,26 |
|
|
LC |
13 |
23 |
43,48 |
|
|
AB |
11 |
23 |
52,17 |
|
|
VL |
15 |
23 |
34,78 |
|
|
DA |
7 |
23 |
69,57 |
|
|
DK |
11 |
23 |
52,17 |
|
|
ST |
8 |
23 |
65,22 |
|
|
EQ |
9 |
23 |
60,87 |
|
|
Total |
- |
112 |
276 |
59,42 |
Conclusiones
Los niveles de ICI,Exp para los laboratorios de química general I y química general II son de 83 y 112 respectivamente. Las prácticas denominadas “Reacciones químicas: ecuaciones químicas” y “Valoraciones ácido-base” representan los experimentos con mayor nivel de riesgo para estos cursos respectivamente.
Los índices evaluados que más aportan al valor final del ICI son los referentes a; la interacción de los compuestos químicos y los valores intrínsecos a las propiedades, como la inflamabilidad y la toxicidad.
Se considera que los valores experimentales del ICI obtenidos para ambos laboratorios son relativamente bajos al compararlos con el valor teórico máximo posible por la metodología utilizada; concluyendo que ambos laboratorios no presentan un nivel de riesgo alto.
Referencias
[1] X. Gao, A. A. Abdul Raman, H. F. Hizaddin, and M. M. Bello, “Systematic review on the implementation methodologies of inherent safety in chemical process,” J. Loss Prev. Process Ind., vol. 65, no. March, p. 104092, 2020, doi: 10.1016/j.jlp.2020.104092.
[2] S. N. H. Husin, A. B. Mohamad, S. R. S. Abdullah, and N. Anuar, “Chemical Health Risk Assessment at The Chemical and Biochemical Engineering Laboratory,” Procedia - Soc. Behav. Sci., vol. 60, no. May 2014, pp. 300–307, 2012, doi: 10.1016/j.sbspro.2012.09.383.
[3] A. Heikkil, “Inherent safety in process plant design, Technical research center of Finland,” pp. 1–132, 1999.
[4] M. Chen, “Process Safety Knowledge Management in the Chemical Process Industry,” Am. J. Chem. Eng., vol. 4, no. 5, p. 131, 2016, doi: 10.11648/j.ajche.20160405.16.
[5] P. Wolkoff, S. T. Larsen, M. Hammer, V. Kofoed-Sørensen, P. A. Clausen, and G. D. Nielsen, “Corrigendum to ‘Human reference values for acute airway effects of five common ozone-initiated terpene reaction products in indoor air’ [Toxicol. Lett. 216 (2013) 54-64],” Toxicol. Lett., vol. 225, no. 3, p. 498, 2014, doi: 10.1016/j.toxlet.2014.01.016.
[6] A. M. Flynn and L. Theodore, Health, Safety, and Accident Management in the Chemical Process Industries. 2002.
[7] J. H. Ware et al., “Respiratory and Irritant Health Effects of Ambient Volatile Organic Compounds,” Am. J. Epidemiol., vol. 137, no. 12, pp. 387–416, 1993, doi: 10.31826/9781463230128-001.
[8] H. B. B. Anuradha, M. Y. Gunasekera, and O. Gunapala, “Comparison of chemical routes based on inherent safety, health and environmental impacts of accidental and daily operational releases,” Process Saf. Environ. Prot., vol. 133, pp. 358–368, 2020, doi: 10.1016/j.psep.2019.11.001.
[9] C. C. Ho and M. S. Chen, “Risk assessment and quality improvement of liquid waste management in Taiwan University chemical laboratories,” Waste Manag., vol. 71, pp. 578–588, 2018, doi: 10.1016/j.wasman.2017.09.029.
[10] P. T. Anastas and D. G. Hammond, Inherent Safety at Chemical Sites: Reducing Vulnerability to Accidents and Terrorism Through Green Chemistry, vol. 16. 2015.
[11] R. Rusli and A. Mohd Shariff, “Qualitative Assessment for Inherently Safer Design (QAISD) at preliminary design stage,” J. Loss Prev. Process Ind., vol. 23, no. 1, pp. 157–165, 2010, doi: 10.1016/j.jlp.2009.07.005.
[12] S. Warnasooriya and M. Y. Gunasekera, “Assessing inherent environmental, health and safety hazards in chemical process route selection,” Process Saf. Environ. Prot., vol. 105, pp. 224–236, 2017, doi: 10.1016/j.psep.2016.11.010.
[13] M. J. Jafari et al., “Exploring inherent process safety indicators and approaches for their estimation: A systematic review,” J. Loss Prev. Process Ind., vol. 52, no. February, pp. 66–80, 2018, doi: 10.1016/j.jlp.2018.01.013.
[14] E. Rodriguez, M. Campinas, J. L. Acero, and M. J. Rosa, “Investigating PPCP Removal from Wastewater by Powdered Activated Carbon/Ultrafiltration,” Water. Air. Soil Pollut., vol. 227, no. 6, 2016, doi: 10.1007/s11270-016-2870-7.
[15] Vargas, X., Benavides, C., Piedra, G., Syedd, R., & Rodríguez, J. (2015). Química Experimental: Un enfoque hacia la Química Verde. Pearson Madrid, España.
[16] Carl Roth - International, 2020. [Online]. Disponible en: https://www.carlroth.com/com/en/. [Accesado: Mayo, 29, 2020].
[17] LabChem Performance through chemistry, 2020. [Online]. Disponible en: https://www.labchem.com/. [Accesado: Mayo, 29, 2020].
[18] Reactivos Química Meyer, 2020. [Online]. Disponible en: http://www.reactivosmeyer.com.mx/. [Accesado: Mayo, 29, 2020].
[19] M. L. Williams, CRC Handbook of Chemistry and Physics, 76th edition.
[20] F. Borgogno, Compendio de Propiedades Tabla de Entalpía de Formación, Energía Libre de Gibbs y Entropía de Formación de Compuestos Inorgánicos. 2010.
[21] A. Saravia et al., “Programa Química General I Laboratorio I Ciclo 2020,” 2020.
[22] M. Esquivel and J. Paniagua, “Programa Química General II Laboratorio II Ciclo 2019.” 2019.
1 Laboratorio de Química de la Atmósfera, Escuela de Química, Facultad de Ciencias Exactas y Naturales, Universidad Nacional. Heredia, Costa Rica. Correo electrónico: jose.mora.barrantes@una.cr https://orcid.org/0000-0002-0409-5276
https://orcid.org/0000-0002-0409-5276
2 Escuela de Química, Facultad de Ciencias Exactas y Naturales, Universidad Nacional. Heredia, Costa Rica. Correo electrónico: jsotomayor.1496@gmail.com https://orcid.org/0000-0002-4824-8756
https://orcid.org/0000-0002-4824-8756
3 Escuela de Química, Facultad de Ciencias Exactas y Naturales, Universidad Nacional. Heredia, Costa Rica. Correo electrónico: christopherf883@gmail.com https://orcid.org/0000-0001-9140-4614
https://orcid.org/0000-0001-9140-4614
4 Escuela de Química, Facultad de Ciencias Exactas y Naturales, Universidad Nacional. Heredia, Costa Rica. Correo electrónico: jlo_acua@hotmail.com https://orcid.org/0000-0003-1345-7563
https://orcid.org/0000-0003-1345-7563
5 Escuela de Química, Facultad de Ciencias Exactas y Naturales, Universidad Nacional. Heredia, Costa Rica. Correo electrónico: mariale.vasa@gmail.com https://orcid.org/0000-0002-5814-4483
https://orcid.org/0000-0002-5814-4483